图1 多极射频发生装置内部结构及其生物学实验示意图
Fig.1 Schematic diagram of the internal structure of the multipolar radiofrequency generator and its biological experiment
摘要 针对多极射频的电极极性排布模式开展研究,建立仿真模型分析皮肤组织中射频能量分布和热量分布随不同处理模式的变化规律,并通过细胞实验和动物实验定量分析了能量分布均匀性对恒功率下多极射频诱导胶原蛋白分泌的影响。结果表明,正、负电极交错排列模式下,多极射频作用于皮肤组织的电流密度均值、能量分布均匀性和热量分布均匀性相对最优。多极射频处理可有效促进体外培养的皮肤成纤维HFF-1细胞增殖并提升细胞活力,同时该应用效果与射频能量分布均匀性正相关。不同电极极性排布模式下多极射频诱导胶原蛋白分泌的效果有显著差异,能量分布均匀性越高,成纤维细胞分泌胶原蛋白量及大鼠皮肤胶原蛋白层厚度增加越明显。以上结果为多极射频技术的临床研究提供了理论和实验支撑。
关键词:多极射频 能量分布 热量分布 胶原蛋白 恒功率
近年来,人们对皮肤健康越发重视,多种无创、非剥脱性方法被开发用于治疗和改善皱纹、松弛、毛细血管扩张、色素沉着等皮肤老化问题[1-5]。其中研究热点技术之一是射频治疗[6-8]。当射频能量作用于人体皮肤组织时,带电粒子在交变电磁场中高速位移产生离子电流,同时大量的极性分子(如H2O等)在高频电场中快速振荡,分子间相互激烈摩擦而产生热量,电场能量转化为热能。射频产生的热量选择性地作用于真皮深层和纤维隔,引起胶原收缩并刺激胶原再生,同时加速真皮及皮下组织的血液循环,促进组织代谢,从而达到减少皱纹、改善皮肤松弛的治疗效果[9-14]。
目前常用的射频设备按照电极结构不同可划分为单极射频、双极射频和多极射频。其中单极射频的正、负两极不在同一界面作用,射频能量从表皮向皮下辐射过程中流向及穿透深度不可控,易造成浅表烧伤、暂时性红斑、炎症后色素沉着等皮肤问题[15]。双极射频的两极端子平行作用于皮肤组织,射频电流流向可控且能量更加集中,但其电流穿透深度(约2 mm)相比于单极射频明显较浅,使得双极射频仅适用于皮肤薄弱部位的治疗[16-17]。多极射频通过动态配置不同极性的多组电极实现射频能量的多点转换,同时可改变电极频率、相位等工作参数,调节射频能量穿透深度,相较于单极/双极系统能量效率显著提高,近年来逐渐成为射频技术研发和推广应用的热点之一。目前多极射频电极直径、间距、频率和相位等参数的控制研究已取得显著突破,通过不同参数配置可有效调控射频能量密度和作用深度,进而实现对特定深度皮肤组织的精准治疗[18-19]。但电极极性排布对多极射频处理效果的影响尚未有相关报道,多极射频电极极性排布的最优配置、作用界面的能量分布均匀性及其皮肤应用的生物学效果亟待研究。
本文首先通过仿真模型研究多极射频不同电极极性排布对皮肤组织中射频能量分布及热量分布的影响规律,再采用细胞生物学和动物实验技术,在细胞和组织水平上定量分析能量分布均匀性对恒功率下多极射频诱导胶原蛋白分泌的影响,同时评估皮肤病理安全性,为后续临床研究提供理论和实验依据。
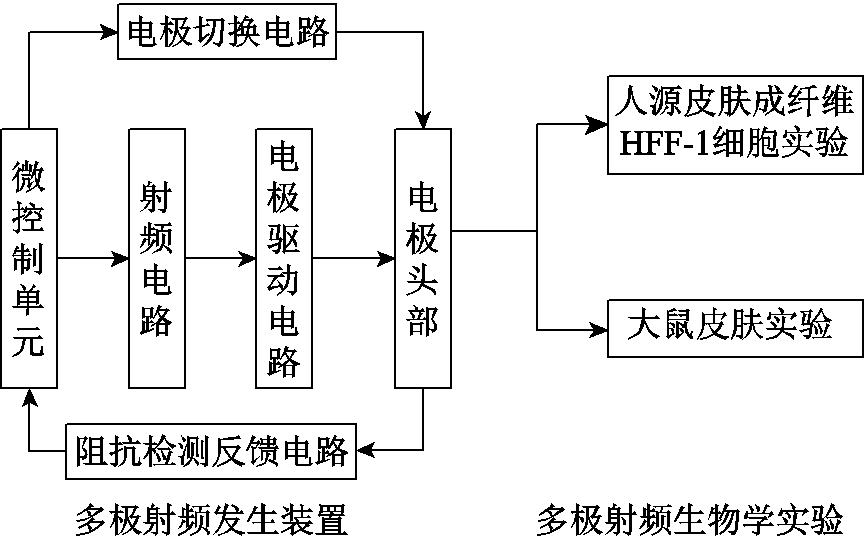
多极射频发生装置内部结构及其生物学实验示意图如图1所示。射频发生装置由微控制单元、射频电路、电极驱动电路、电极切换电路、阻抗检测反馈电路和电极头部组成。射频发生装置的电路模块和电极头部由西安电子科技大学和西安拾玖岁信息科技有限公司自主研发。电极驱动电路对射频电路产生的高频交流信号进行升压,向多极射频提供高频高压交流信号。电极切换电路协同微控制单元实现多极射频的电极极性切换控制。阻抗检测反馈电路用于检测多组电极部位的皮肤阻抗值,与微控制单元协作完成多极射频处理温度的稳定性及均衡性控制。该反馈回路可以延长多极射频在设定温度下的处理时间,减小目标组织过热和相关不利因素的影响[20-21]。

图1 多极射频发生装置内部结构及其生物学实验示意图
Fig.1 Schematic diagram of the internal structure of the multipolar radiofrequency generator and its biological experiment
多极射频发生装置电路模块及电极头部如图2所示。电极头部设计为三行三列的矩形对称点阵结构,电极数量为9个,电极直径为5 mm,电极间距4 mm。针对每个电极都设置有独立通路,可单独控制电极频率、正负极性、射频波形等参数。多极射频的每一个电极都可在正电极、负电极、悬空等工作状态之间切换,从而形成不同的电极极性排布模式。图3展示了本文重点研究的三种电极极性排布模式,在电极模式1中,每一行电极的极性相同,相邻两行电极的极性相反;在电极模式2中,正、负电极交错排列;在电极模式3中,每一行/列有两电极极性相同,上、下两电极极性相反。
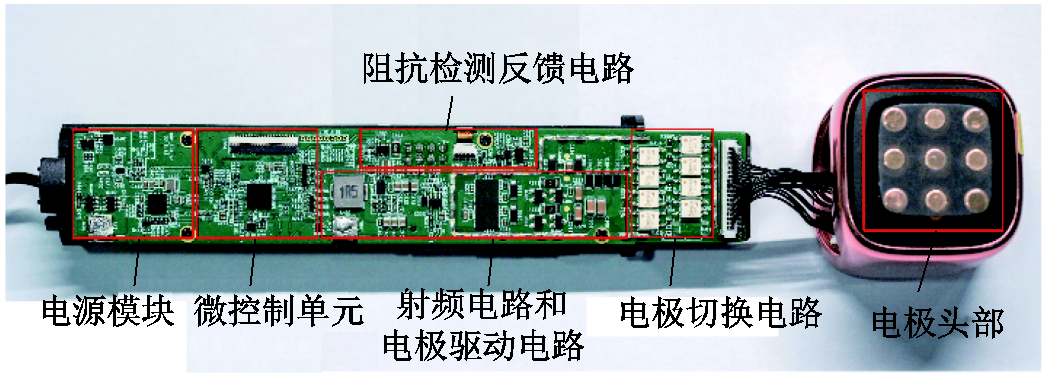
图2 多极射频发生装置电路模块及电极头部
Fig.2 Circuit module and electrode head of multipolar radiofrequency generator
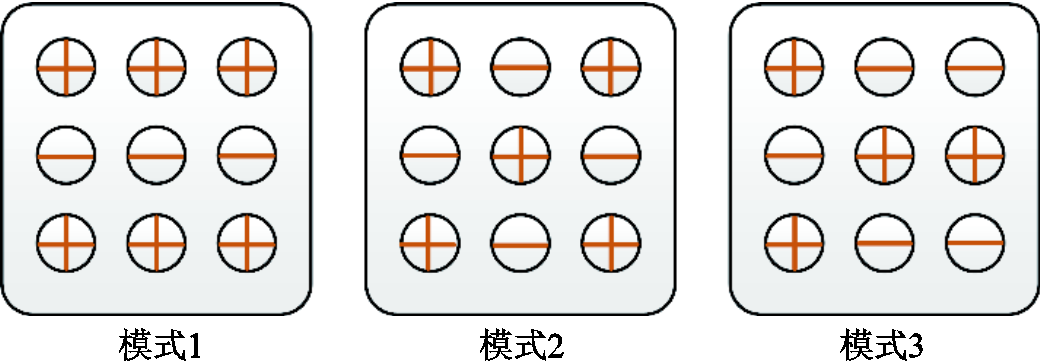
图3 多极射频的三种电极极性排布模式
Fig.3 Three electrode polarity arrangement modes of multipolar radiofrequency
在本文实验中,多极射频的恒定输出功率为8 W,射频峰值电压为80 V,频率为1 MHz。
在细胞生物学实验中,多极射频处理体外培养的人源皮肤成纤维HFF-1细胞,研究不同电极极性排布模式对细胞增殖、细胞活性以及诱导胶原蛋白分泌的影响,具体过程如下。
人源皮肤成纤维细胞HFF-1购自国家生物医学实验细胞资源库,在含10%胎牛血清的DMEM培养液(Corning, Cat. 10-013-CVR,US)中,于温度37℃、浓度5%的二氧化碳培养箱(Thermo 371, US)中培养。取对数生长期的HFF-1接种在直径为 35 mm的培养皿中(2×105个/皿)构建2D单层细胞模型,分为2个对照组和3个实验组。
第一对照组不进行射频等任何处理,第二对照组仅进行短暂的42 ℃水浴处理。实验组分别用多极射频的三种电极极性排布模式处理细胞模型。多极射频输出功率固定为8 W,射频电极表面温度设定为42 ℃,达到预设温度后每次处理2 min,每天处理1次,连续处理3天。处理24 h后,经胰酶消化制成均匀的单细胞悬液。将10 μL细胞悬液加入到血球计数板,应用倒置显微镜(Olympus IX51, Japan)观察细胞形态并计数,绘制细胞生长图表。将细胞悬液和CellTiter-Glo试剂(Promega, Cat. G7570, US)等比例混合,室温孵育10 min后,使用多功能酶标仪(Thermo VARIOSKAN FLASH,US)检测细胞活性。采用总胶原蛋白试剂盒(Total Collagen Assay Kit (Colorimetric), Biovision, Cat. K218-100, US)检测细胞分泌胶原蛋白的水平。所有实验均独立重复3次。
在动物生物学实验中,多极射频处理大鼠背部皮肤,研究不同电极极性排布模式对大鼠皮肤诱导胶原蛋白分泌及皮肤病理安全性的影响,具体过程如下。
本实验选用20只30日龄雌性SD(Sprague Dawley)大鼠(购自西安交通大学实验动物中心),大鼠初始体重为(100±8)g,使用剃毛刀及脱毛膏脱去大鼠背部靠近尾部处背毛。将大鼠随机分为4组(n=5),对照组不进行射频等任何处理,实验组分别用多极射频的三种电极极性排布模式处理大鼠背部皮肤。所有大鼠每天处理1次,连续26天。多极射频输出功率固定为8 W,射频电极表面温度设定为42℃(射频能量输出时不会烫伤皮肤表皮),达到预设温度后每次治疗2 min。所有大鼠饲养条件标准统一,射频处理过程中大鼠体重正常增长,且对照组与各处理组之间无显著性差异。
完成射频治疗后,伦理处死所有大鼠,切取对照组与各实验组射频治疗区皮肤组织。将取下来的皮肤组织经4%多聚甲醛固定,固定状态良好后,对组织进行修剪、脱水、包埋、切片、染色、封片,最后镜检合格的样片。通过Masson染色(Servicebio, Cat. G1006, China)观察测量皮肤胶原纤维含量变化,Masson染色后胶原纤维呈蓝色,肌纤维呈红色。通过HE染色(Servicebio, Cat. G1003, China)观察皮肤组织变化,评估皮肤病理损伤。使用PANNORAMIC全景切片扫描仪(3DHISTECH(Hungary))对图像进行采集。成像完成后使用Image-Pro Plus 6.0分析软件,统一以mm作为标准单位,随机测量每张切片中5处胶原层厚度,并计算出平均值。
采用SPSS 20.0软件对不同处理组细胞数量、细胞活力、总胶原蛋白浓度以及大鼠皮肤胶原层厚度进行t检验分析,当p<0.05时被认为差异有统计学意义(*p<0.05, **p<0.01, ***p<0.001)。计量资料描述用均数±标准差 (Mean±SD) 表示。
本文采用COMSOL Multiphysics软件建立了多极射频作用于皮肤组织的三维仿真模型,研究不同电极极性排布模式对恒功率下射频能量分布及皮肤组织中热量分布的影响规律。仿真模型耦合电场、固体传热和多物理场电磁热多个模块[22-23]。模型几何结构如图4所示。图4中,皮肤组织模型分为皮肤层、脂肪层和肌肉层三部分,射频电极头部与皮肤层直接接触。射频电极和皮肤组织模型的几何尺寸见表1。皮肤组织模型各部分物理属性见表2,其中物理参数来源于基础物理实验,并已被J. Jiménez-Lozano [24]和González-Suárez [25]等研究人员采用。仿真模型中的射频参数与实验条件一致,射频峰值电压为80 V,频率为1 MHz,计算时长为2 min。在t=0时刻,假定环境温度为293 K,皮肤组织温度为308 K,射频电极初始温度与环境温度一致。
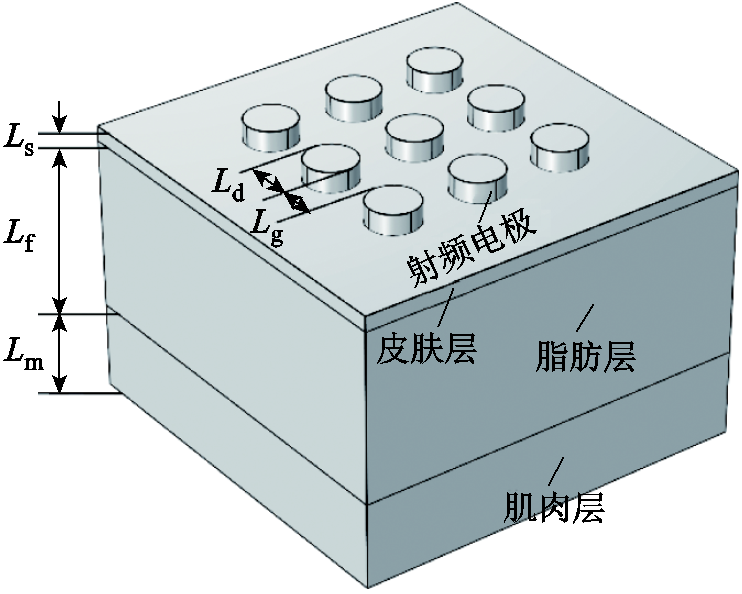
图4 模型几何结构
Fig.4 The geometric structure of the model
表1 模型几何尺寸
Tab.1 Model geometry

参数数值/mm Ls1.5 Lf17 Lm8.5 Ld5 Lg4
表2 模型各部分物理属性
Tab.2 Physiological properties of model different regions
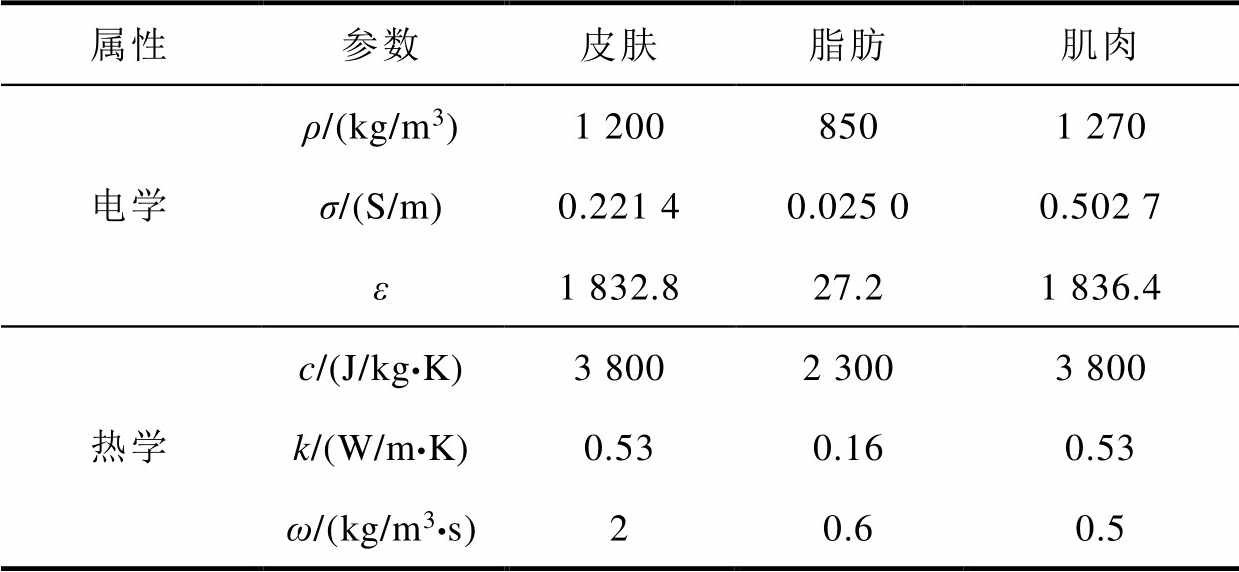
属性参数皮肤脂肪肌肉 电学ρ/(kg/m3)1 2008501 270 σ/(S/m)0.221 40.025 00.502 7 ε1 832.827.21 836.4 热学c/(J/kg•K)3 8002 3003 800 k/(W/m•K)0.530.160.53 ω/(kg/m3•s)20.60.5
图5a展示了多极射频不同电极极性排布模式下皮肤层1 mm处的电流密度分布,其中三种处理模式与图3相互对应。在模式1中,多极射频每一行电极的极性相同,相邻两行电极的极性相反,射频能量集中分布在相邻两行电极间,电流密度最大值(550 A/m2)明显高于模式2和模式3。在模式2中,多极射频的正、负电极交错排列,射频能量较均匀地分布在相邻两电极之间,电流密度最大值相对最小(446 A/m2)。在电极模式3中,多极射频每一行/列有两电极极性相同,上、下两电极极性相反,射频能量较集中分布在相邻两正、负电极之间。
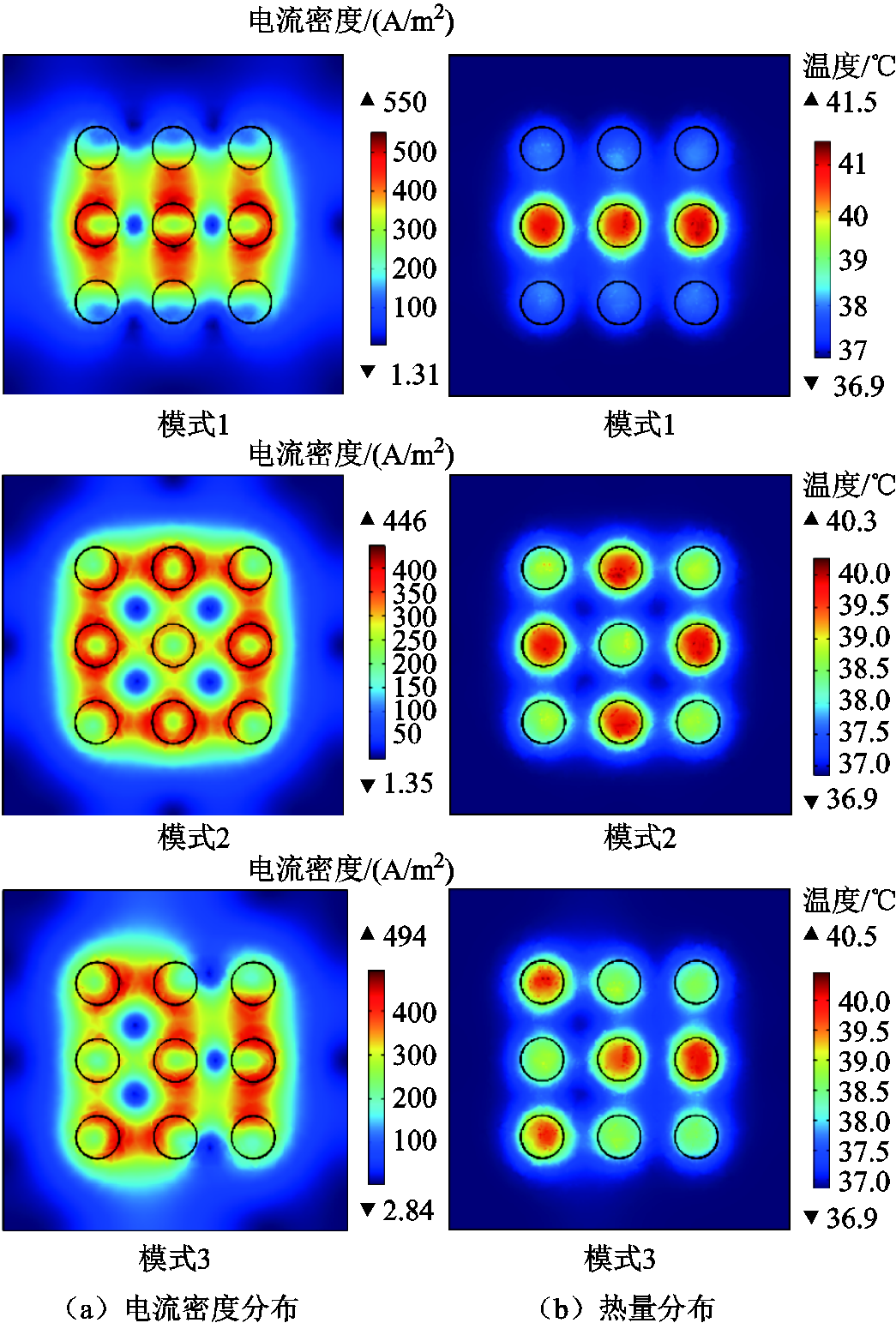
图5 多极射频不同电极极性排布模式下皮肤层1 mm处的电流密度分布和热量分布
Fig.5 Current density distribution and heat distribution at 1 mm of skin layer under different electrode polarity arrangement modes of multipolar radiofrequency
为了进一步定量比较不同电极极性排布模式下射频能量分布均匀性,本文均匀提取了皮肤层1 mm处多极射频作用界面的100个电流密度数据点,统计分析数据见表3。结果显示,虽然模式2对应的射频电流密度最大值相对最小,但作用界面内的电流密度均值相对最大。通过定量比较,在三种不同电极极性排布模式下,多极射频电流密度均值大小排列为:模式2≈模式3>模式1,多极射频能量分布均匀性(以标准差数据体现)由好到差依次排列为:模式2>模式3>模式1。该结果反映出,正、负电极交错排列模式下,多极射频的电流密度均值和能量分布均匀性相对最优。
表3 多极射频不同电极极性排布模式下皮肤层1 mm处电流密度统计表
Tab.3 Statistical table of current density at 1 mm of skin layer under different electrode polarity arrangement modes of multipolar radiofrequency

组别样本量电流密度/(A/m2)标准差 平均值最小值最大值 模式1100246.4722.18549.32168.26 模式2100291.8933.01445.1495.63 模式3100292.1323.16492.68129.51
图5b展示了多极射频不同电极极性排布模式下皮肤层1 mm处的温度分布。结果显示,多极射频能量作用下,皮肤组织层的温度分布具有显著不均匀性,热量主要集中在电极个数相对较少的正、负电极对应位置。以模式1为例,正、负电极数量差异最为明显,热量主要集中分布在3个负极性电极对应位置。在电极极性排布模式1下,皮肤层1 mm处温度最高值达到41.5 ℃,明显大于模式2和模式3中的温度最高值。
为了进一步定量比较不同电极极性排布模式下射频电流作用于皮肤组织的热量分布均匀性,本文均匀提取了皮肤层1 mm处多极射频作用界面的100个温度数据点,统计分析数据见表4。结果显示,在三种不同电极极性排布模式下,多极射频作用于皮肤组织的温度均值大小排列为:模式2≈模式3>模式1,温度分布均匀性(以数据标准差体现)由好到差依次排列为:模式2>模式3>模式1。该结果与图5a和表3中射频能量分布均匀性结果一致,正、负电极交错排列模式下,多极射频作用于皮肤组织的温度均值和温度分布均匀性相对最优。
表4 多极射频不同电极极性排布模式下皮肤层1 mm处温度统计表
Tab.4 Statistical table of temperature at 1 mm of skin layer under different electrode polarity arrangement modes of multipolar radiofrequency
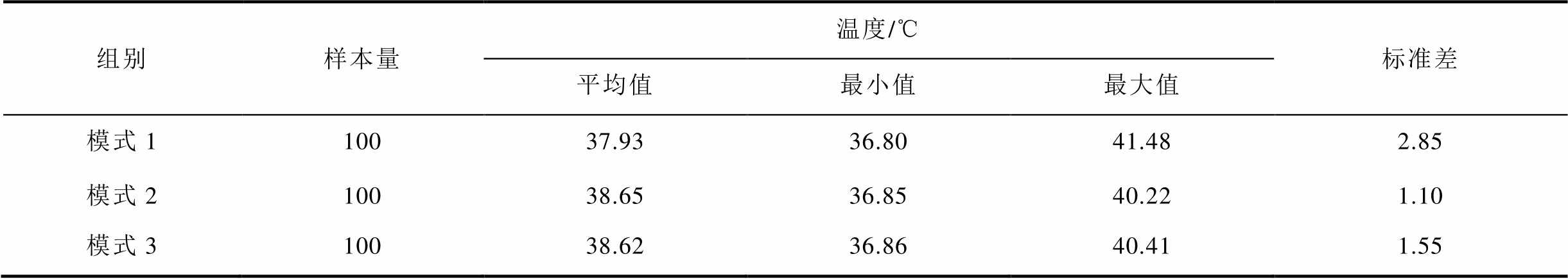
组别样本量温度/℃标准差 平均值最小值最大值 模式110037.9336.8041.482.85 模式210038.6536.8540.221.10 模式310038.6236.8640.411.55
当多极射频作用于人体皮肤时,射频电流从正极性电极流经皮肤后返回负极性电极,通过皮肤组织的电阻效应在传播回路中产生热量。该过程中,正极流出总电流和负极电流大小相等。针对不同电极极性排布模式,当正/负极性电极数量不相等时,数量相对较少的正/负电极对应位置处射频电流密度较大,电阻效应下的焦耳加热效应更为显著,所在位置的皮肤组织产生热量及温度也会更高。以上模型计算结果证明,不同电极极性排布模式会对恒功率下射频能量分布及皮肤组织中热量分布产生显著影响,正负电极交错排列模式下,能量分布及温度分布均匀性相对最优。值得一提的是,由于多极射频频率和相位固定不变,因此本文实验中多极射频能量作用深度(约3.5 mm)基本未受到电极极性排布模式的影响。
固定射频输出功率8 W和电极表面温度42℃,多极射频在不同电极极性排布模式下处理人源皮肤成纤维HFF-1细胞,HFF-1细胞增殖和活力随电极极性模式的变化如图6所示。
与对照组相比,多极射频在模式1、模式2和模式3条件下处理体外培养的HFF-1细胞后,均可促进细胞增殖,处理并孵育24 h后可分别增加细胞数量约2.1%、4.2%和3.5%。进一步的细胞活力监测表明,三种模式下的多极射频处理成纤维细胞后,可分别提高HFF-1细胞活力约5.8%、11.5%和7.9%。利用42℃恒温水浴加热来模拟多极射频的热处理过程,发现42℃热刺激同样可以在一定程度上促进HFF-1细胞增殖和活力提升,但该效果要明显弱于多极射频处理。上述实验结果表明,多极射频的恒温处理(42℃)可有效促进体外培养的成纤维HFF-1细胞增殖并提升细胞活力,且不同处理模式的应用效果差异显著。现有研究指出,一定条件的热刺激可有效提高细胞与周围环境的物质交换速率,并加快细胞代谢水平[6-7, 19]。而多极射频对细胞的促增殖和活性提升效应,正是通过其诱导的热效应来实现的。另外,通过对比不同电极极性排布模式下多极射频对HFF-1细胞的刺激效应,发现能量分布更加均匀的模式2多极射频的作用效果更加显著,这一结果表明多极射频的应用效果与射频能量分布均匀性正相关。
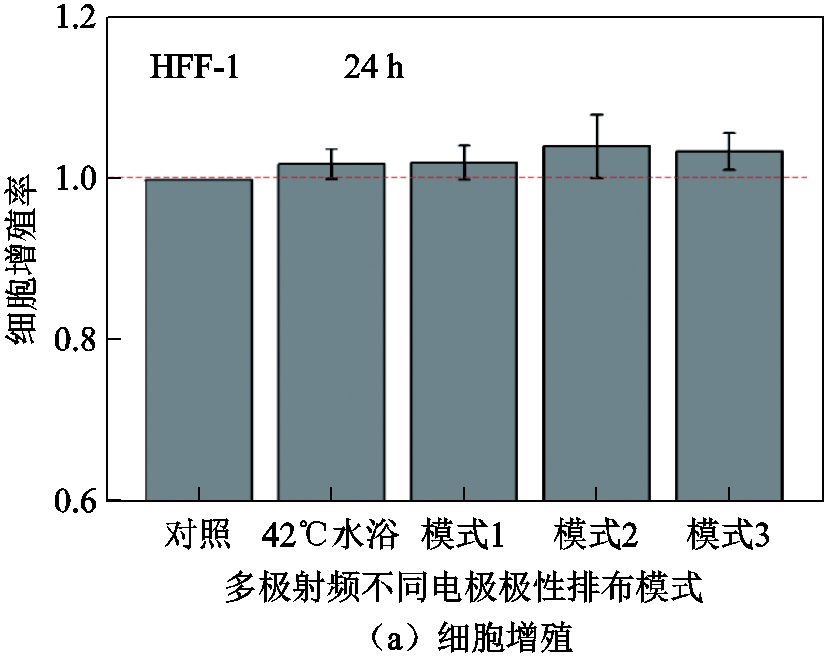
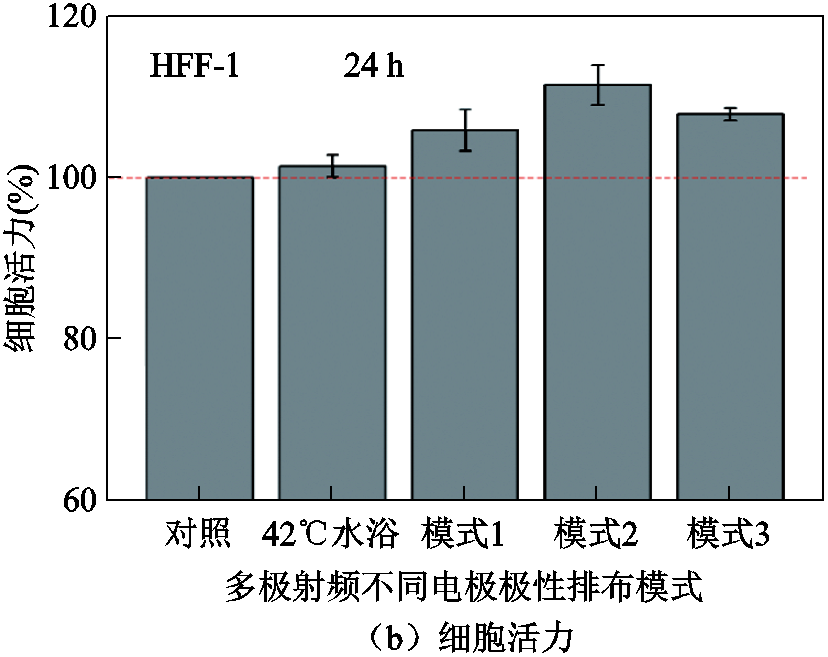
图6 多极射频不同处理模式下人源皮肤成纤维HFF-1细胞增殖和活力的变化
Fig.6 Changes in proliferation and viability of human skin fibroblast HFF-1 cells under different treatment modes of multipolar radiofrequency
此外,进一步研究了多极射频不同电极极性排布模式对成纤维HFF-1细胞胶原蛋白分泌的影响,研究结果如图7所示。多极射频的不同处理模式对细胞分泌胶原蛋白有明显的调控差异,在上述三种射频电极极性排布模式中,仅模式2可显著提高总胶原蛋白分泌量达9.1%,而电极极性排布模式1和模式3却不同程度地降低了总胶原蛋白分泌量。相较于对照组,当多极射频电流密度均值提高15.5%时(从模式1到模式2),体外培养的成纤维HFF-1细胞分泌总胶原蛋白量可增加约11.1%,而42℃恒温水浴刺激并未对成纤维HFF-1细胞分泌胶原蛋白产生明显影响。
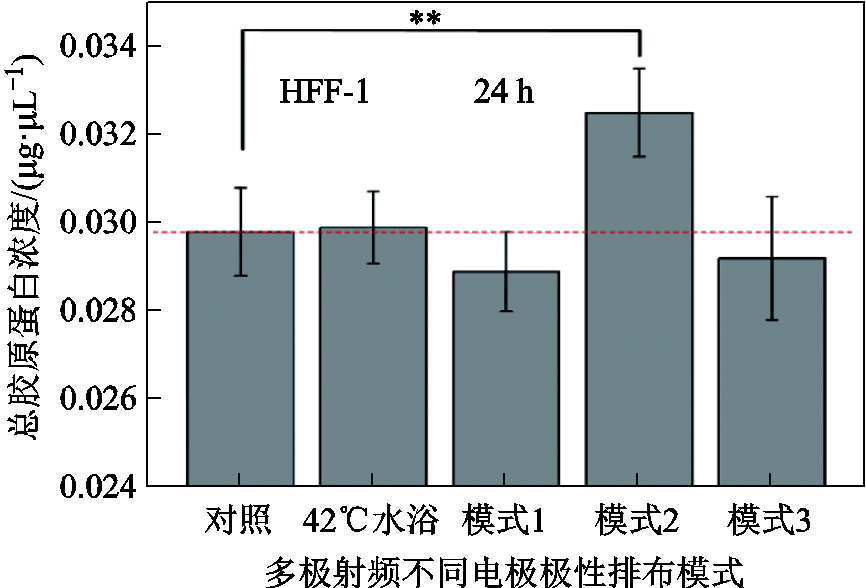
图7 多极射频不同处理模式下人源皮肤成纤维HFF-1细胞胶原蛋白分泌量的变化
Fig.7 Changes in collagen secretion from human skin fibroblast HFF-1 cells under different treatment modes of multipolar radiofrequency
在多极射频处理过程中,射频能量转化为热能作用于成纤维细胞及其分泌的胶原蛋白分子。人皮肤组织中的胶原蛋白由三条多肽链组成,并通过氢键相连呈三螺旋结构。射频转化的热量一方面可以破坏氢键及多肽交联链,使得胶原蛋白从高度有序的晶体结构转变为随机的凝胶状态(变性);另一方面射频热能会刺激细胞外基质成分变化,促进成纤维细胞分泌新的胶原蛋白[8, 26-27]。D. Kist等曾研究发现,射频能量密度和作用次数的增加都可促进胶原变性,但低能量的多次治疗累积效果优于高能量的单次治疗效果[28]。B. D. Zelickson等实验证明了射频能量会导致胶原纤维出现即刻收缩现象,治疗后两天胶原mRNA水平为对照组的2.4倍[29]。本文研究表明42℃恒温水浴虽然可以提升HFF-1细胞活力,但并未对HFF-1细胞胶原蛋白分泌量产生影响。这表明并不是所有外源热量都可以有效刺激成纤维细胞分泌胶原蛋白,极性分子和带电离子在高频电场中的振荡运动可能在射频能量促进细胞分泌胶原蛋白中发挥关键作用。而多极射频的不同电极极性排布模式对诱导细胞分泌胶原蛋白方面有显著差异,进一步表明射频能量分布均匀性和热量分布均匀性可能是诱导细胞分泌胶原蛋白的重要参数,更高的能量分布均匀性在促进成纤维细胞增殖、提高细胞活力、诱导细胞胶原蛋白分泌方面有突出优势。以上结果对多极射频技术后续的细胞生物学实验有重要的指导意义。
最后,本文研究了多极射频不同电极极性排布模式对大鼠皮肤分泌胶原蛋白及皮肤病理安全性的影响。其中多极射频不同处理模式下大鼠皮肤Masson染色扫描图和胶原蛋白层厚度变化结果分别如图8和图9所示。
大鼠皮肤Masson染色结果显示,实验组大鼠皮肤胶原增生变厚明显,不同电极极性排布模式下多极射频处理大鼠皮肤都可以有效增加胶原蛋白厚度,且皮肤胶原层结构均正常(图8中黑色线段及箭头示意处为大鼠皮肤胶原蛋白层)。与对照组相比,多极射频在模式1下连续处理大鼠皮肤26天,大鼠皮肤胶原蛋白层平均厚度增加约0.02 mm。模式2的作用效果最为突出,26天后大鼠皮肤胶原蛋白层平均厚度增加约0.13 mm。在电极极性排布模式3下,多极射频处理可增加大鼠皮肤胶原蛋白层平均厚度约0.06 mm。具体对比而言,当多极射频电流密度均值提高15.5%时(从模式1转换到模式2),大鼠皮肤胶原蛋白层厚度可增加约12.3%。结合图5的仿真模型结果,该实验结果表明,多极射频作用界面的能量分布均匀性越高,大鼠皮肤胶原蛋白层厚度增加越显著。
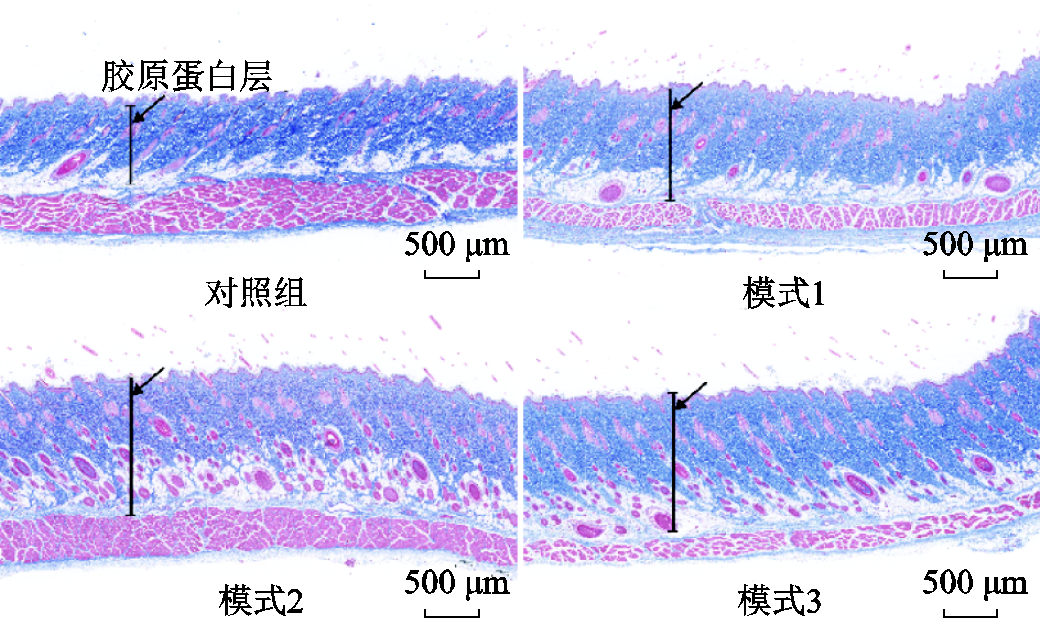
图8 多极射频不同处理模式下大鼠皮肤Masson染色扫描图
Fig.8 Masson staining scans of rat skin under different treatment modes of multipolar radiofrequency
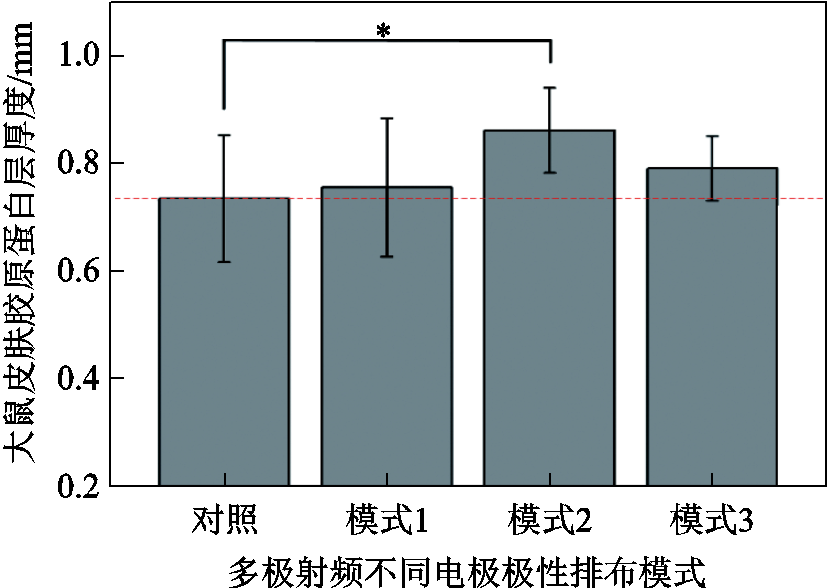
图9 多极射频不同处理模式下大鼠皮肤胶原蛋白层厚度的变化
Fig.9 Changes in collagen layer thickness in rat skin under different treatment modes of multipolar radiofrequency
此外,本文评估了多极射频在不同电极极性排布模式下的皮肤处理生物安全性,其中大鼠皮肤HE病理切片结果如图10所示。病理分析结果表明,各实验组大鼠皮肤真皮无病变、无真皮结缔组织血管扩张充血或水肿、无真皮炎性细胞浸润、无表皮坏死无棘层肥厚等现象。该结果表明本研究的多极射频实验装置工作在不同电极极性排布模式下均不会影响大鼠皮肤的病理安全性,射频能量分布均匀性的调控效果主要体现在深层皮肤加热及其胶原蛋白分泌的影响。

图10 多极射频不同处理模式下大鼠皮肤HE病理切片(5.0×表示放大倍数5倍,20.0×表示放大倍数20倍)
Fig.10 HE pathological sections of rat skin under different treatment modes of multipolar radiofrequency (5.0× means 5 times magnification, 20.0×means 20 times magnification)
射频治疗的多项研究曾指出,射频电流对皮肤胶原分泌的影响主要依赖组织导电性及热效应累积。当射频电流经过人体组织时,皮肤及皮下组织成为导电体,带电粒子在交变电磁场中的位移产生离子电流,同时组织细胞内水分子在高频电磁场中快速振荡摩擦而产生热量。以上相互作用导致电磁能量耗散,升高了皮肤组织的温度,通过组织热效应达到治疗效果。热效应的大小取决于皮肤阻抗的大小和射频电流强度、分布以及处理时间[6, 30]。例如,D. J. Goldberg等曾报道皮肤组织热损伤会启动创伤愈合应答,激发成纤维细胞活性,促进新胶原蛋白形成,进而实现真皮的重建和增厚[31]。B. D. Zelickson等曾证实射频能量可以使局部皮肤成纤维细胞增生活跃,增加真皮中深层胶原纤维[29]。本研究在细胞和组织水平上进一步证实了多极射频对皮肤组织胶原蛋白分泌的促进作用。更关键的是,本文发现不同电极极性排布对多极射频的皮肤热效应有显著差异。不同电极极性排布模式改变了多极射频电流路径及皮肤组织内部的能量分布和热量分布,继而可能导致皮肤内部粒子运动、pH值以及其他更为复杂参数的变化,使得多极射频在更高能量分布均匀性的情况下产生更为突出的皮肤热效应,皮肤胶原蛋白分泌量显著提高。不同电极极性排布模式并不会影响多极射频治疗的皮肤病理安全性,意味着皮肤浅层对这种皮肤热效应变化并不敏感。
本文通过仿真模型和生物学实验定量研究了不同电极排布模式对恒功率下多极射频能量分布及诱导皮肤胶原蛋白分泌的影响,得出以下结论:
1)正负电极交错排列模式下,多极射频作用于皮肤组织的电流密度均值、能量分布均匀性和热量分布均匀性相对最优。
2)多极射频处理可有效促进体外培养的成纤维HFF-1细胞增殖并提升细胞活力,同时射频能量分布均匀性对诱导细胞分泌胶原蛋白具有显著影响。
3)多极射频处理可有效增加大鼠皮肤胶原蛋白层厚度,作用界面的能量分布均匀性越高,胶原蛋白层厚度增加越显著,该作用过程不影响大鼠皮肤的病理安全性。
本文研究表明不同电极极性排布模式导致皮肤内部粒子运动、热量分布等参数发生变化,是影响多极射频诱导胶原蛋白分泌能力的关键因素。多极射频在更高能量分布均匀性的情况下产生更为突出的皮肤热效应,为后续临床研究提供了理论和实验支撑。
参考文献
[1] Alexis A F, Obioha J O. Ethnicity and aging skin[J]. Journal of Drugs in Dermatology: JDD, 2017, 16(6): s77-s80.
[2] 杨帆, 余晓, 刘黎, 等. 基于太赫兹时域光谱技术的皮肤水分含量评估[J]. 电工技术学报, 2021, 36(4): 777-786. Yang Fan, Yu Xiao, Liu Li, et al. Water content evaluation of skin tissue based on terahertz time domain spectroscopy[J]. Transactions of China Electrotechnical Society, 2021, 36(4): 777-786.
[3] Kammeyer A, Luiten R M. Oxidation events and skin aging[J]. Ageing Research Reviews, 2015, 21: 16-29.
[4] 苑曦宸, 张彬, 孟智悦, 等. 磁场促进生物体内氧气利用的机制及其医学应用[J]. 电工技术学报, 2021, 36(4): 676-684. Yuan Xichen, Zhang Bin, Meng Zhiyue, et al. Mechanism of magnetic field promoting oxygen utilization in organism and its medical application[J]. Transactions of China Electrotechnical Society, 2021, 36(4): 676-684.
[5] Pritzker R N, Hamilton H K, Dover J S. Comparison of different technologies for noninvasive skin tightening[J]. Journal of Cosmetic Dermatology, 2014, 13(4): 315-323.
[6] Augustyniak A, Rotsztejn H. Nonablative radiofrequency treatment for the skin in the eye area - clinical and cutometrical analysis[J]. Journal of Cosmetic Dermatology, 2016, 15(4): 427-433.
[7] 臧连儒, 周宇, 康佳, 等. 电极间距与电极直径对恒功率下双极射频熔脂效果影响的研究[J]. 中国生物医学工程学报, 2020, 39(5): 566-576. Zang Lianru, Zhou Yu, Kang Jia, et al. Study on the effect of electrode spacing and electrode diameter on bipolar radiofrequency fat melting at constant power[J]. Chinese Journal of Biomedical Engineering 2020, 39(5): 566-576.
[8] 张帅, 许家悦, 李梦迪, 等. 基于皮层神经元模型的经颅磁声电刺激神经网络放电活动仿真分析[J]. 电工技术学报, 2021, 36(18): 3851-3859. Zhang Shuai, Xu Jiayue, Li Mengdi, et al. Simulation of the discharge activity of neural network under transcranial magneto-acousto-electrical stimulation based on cortical neuron model[J]. Transactions of China Electrotechnical Society, 2021, 36(18): 3851-3859.
[9] Belenky I, Margulis A, Elman M, et al. Exploring channeling optimized radiofrequency energy: a review of radiofrequency history and applications in esthetic fields[J]. Advances in Therapy, 2012, 29(3): 249-266.
[10] 刘丽红, 杨蓉娅. 射频技术原理及在皮肤美容科的应用进展[J]. 中国激光医学杂志, 2008, 17(4): 292-295. Liu Lihong, Yang Rongya.radiofrequency technology in cosmetic dermatology: its advancement[J]. Chinese Journal of Laser Medicine & Surgery, 2008, 17(4): 292-295.
[11] 吴秋菊, 周展超, 林彤, 等. 射频技术治疗面颈部皮肤皱纹和松弛的临床疗效观察[J]. 中华皮肤科杂志, 2008, 41(5): 318-320. Wu Qiuju, Zhou Zhanchao, Lin Tong, et al. Clinical efficacy of radiofrequency for skin wrinkles and laxity on the face and neck[J]. Chinese Journal of Dermatology, 2008, 41(5): 318-320.
[12] Wilczyński S, Stolecka-Warzecha A, Deda A, et al. In vivo dynamic thermal imaging of skin radiofrequency treatment[J]. Journal of Cosmetic Dermatology, 2019, 18(5): 1307-1316.
[13] Gold M, Andriessen A, Bader A, et al. Review and clinical experience exploring evidence, clinical efficacy, and safety regarding nonsurgical treatment of feminine rejuvenation[J]. Journal of Cosmetic Dermatology, 2018, 17(3): 289-297.
[14] Meyer P F, de Oliveira P, Silva F K B A, et al. Radiofrequency treatment induces fibroblast growth factor 2 expression and subsequently promotes neocollagenesis and neoangiogenesis in the skin tissue[J]. Lasers in Medical Science, 2017, 32(8): 1727-1736.
[15] Kaplan H, Gat A. Clinical and histopathological results following TriPollar™ radiofrequency skin treatments[J]. Journal of Cosmetic and Laser Therapy, 2009, 11(2): 78-84.
[16] 郭丽芳, 林彤, 黄玉清, 等. 点阵双极射频技术治疗面颈部皱纹的疗效与安全性评价[J]. 中华皮肤科杂志, 2014, 47(10): 695-698. Guo Lifang, Lin Tong, Huang Yuqing, et al. Assessment of efficacy and safety of a bipolar fractionated radiofrequency device for the treatment of wrinkles of the face and neck[J]. Chinese Journal of Dermatology, 2014, 47(10): 695-698.
[17] Friedmann D P. A review of the aesthetic treatment of abdominal subcutaneous adipose tissue[J]. Dermatologic Surgery, 2015, 41(1): 18-34.
[18] Franco W, Kothare A, Ronan S J, et al. Hyperthermic injury to adipocyte cells by selective heating of subcutaneous fat with a novel radiofrequency device: feasibility studies[J]. Lasers in Surgery and Medicine, 2010, 42(5): 361-370.
[19] Bonjorno A R, Gomes T B, Pereira M C, et al. Radiofrequency therapy in esthetic dermatology: a review of clinical evidences[J]. Journal of Cosmetic Dermatology, 2020, 19(2): 278-281.
[20] 米彦, 陈嘉诚, 许宁, 等. 基于辅助充电支路的模块化多电平变换器结构高频纳秒脉冲发生器[J]. 电工技术学报, 2021, 36(2): 435-444. Mi Yan, Chen Jiacheng, Xu Ning, et al. High frequency nanosecond pulse generator based on modular multilevel converter structure with auxiliary charging branch[J]. Transactions of China Electrotechnical Society, 2021, 36(2): 435-444.
[21] 马静, 米超, 夏冰阳, 等. 基于负序功率正反馈的孤岛检测新方法[J]. 电工技术学报, 2013, 28(4): 191-195. Ma Jing, Mi Chao, Xia Bingyang, et al. A novel islanding detection method based on negative-sequence power positive feedback[J]. Transactions of China Electrotechnical Society, 2013, 28(4): 191-195.
[22] 米彦, 彭文成, 芮少琴, 等. 高频纳秒脉冲串作用下皮肤肿瘤热效应的多参数有限元仿真与实验[J]. 电工技术学报, 2017, 32(22): 264-274. Mi Yan, Peng Wencheng, Rui Shaoqin, et al. Thermal effects in skin tumor exposed to high-frequency nanosecond pulse bursts: multi-parametric finite element simulation and experiment[J]. Transactions of China Electrotechnical Society, 2017, 32(22): 264-274.
[23] 胡亚楠, 包家立, 朱金俊, 等. 纳秒电脉冲对肝脏组织不可逆电穿孔消融区分布的时域有限差分法仿真[J]. 电工技术学报, 2021, 36(18): 3841-3850. Hu Yanan, Bao Jiali, Zhu Jinjun, et al. The finite difference time domain simulation of the distribution of irreversible electroporation ablation area in liver tissue by nanosecond electrical pulse[J]. Transactions of China Electrotechnical Society, 2021, 36(18): 3841-3850.
[24] Jiménez-Lozano J, Vacas-Jacques P, Anderson R R, et al. Selective and localized radiofrequency heating of skin and fat by controlling surface distributions of the applied voltage: analytical study[J]. Physics in Medicine and Biology, 2012, 57(22): 7555-7578.
[25] González-Suárez A, Gutierrez-Herrera E, Berjano E, et al. Thermal and elastic response of subcutaneous tissue with different fibrous septa architectures to RF heating: numerical study[J]. Lasers in Surgery and Medicine, 2015, 47(2): 183-195.
[26] Harth Y, Lischinsky D. A novel method for real-time skin impedance measurement during radiofrequency skin tightening treatments[J]. Journal of Cosmetic Dermatology, 2011, 10(1): 24-29.
[27] Tay Y K, Kwok C. A novel radiofrequency device for the treatment of rhytides and lax skin: a pilot study[J]. Journal of Cosmetic and Laser Therapy, 2009, 11(1): 25-28.
[28] Kist D, Burns A J, Sanner R, et al. Ultrastructural evaluation of multiple pass low energy versus single pass high energy radio-frequency treatment[J]. Lasers in Surgery and Medicine, 2006, 38(2): 150-154.
[29] Zelickson B D, Kist D, Bernstein E, et al. Histological and ultrastructural evaluation of the effects of a radiofrequency-based nonablative dermal remodeling device[J]. Archives of Dermatology, 2004, 140(2).
[30] Emilia del Pino M, Rosado R H, Azuela A, et al. Effect of controlled volumetric tissue heating with radiofrequency on cellulite and the subcutaneous tissue of the buttocks and thighs[J]. Journal of Drugs in Dermatology: JDD, 2006, 5(8): 714-722.
[31] Goldberg D J. Laser and lights[M]. Philadelphia: Elsevier Saunders, 2005.
Abstract Radiofrequency (RF) treatments, where heat selectively acts on skin tissue, are widely used to treat and improve wrinkles, capillary dilation, hyperpigmentation and other skin problems.The penetration depth and distribution uniformity of RF energy can beregulated by adjusting the electrode frequency, phase and polarity of multipolar RF parameters, which can significantly improve the energy efficiency compared withmonopolar RF and bipolar RF. In recent years, parameters such as electrode diameter, frequency or phase of multipolar RF have been extensively studied, but the effect of different electrode polarity arrangements on the therapeutic effect has rarely been reported. The aim of this paper is to investigate the effect of the electrode polarity arrangement modes of multipolar RF on the uniformity of energy distribution and its biological effect on skin application.
Firstly, a three-dimensional simulation model isestablished using COMSOL Multiphysics software to investigate the effect of three electrode polarity arrangement modes of multipolar RF on energy distribution and heat distribution in skin tissue at constant power. In mode 1, the polarity of each row of electrodes is the same and the polarity of two adjacent rows is opposite. In mode 2, the positive and negative electrodes are staggered. In mode 3, each row/column has two electrodes of the same polarity, while the top and bottom electrodes have opposite polarities.The simulation model couples several physical field modules,including electric field, solid heat transfer and electromagnetic heat, where the electrical and thermal parameters of the skin tissue are referred to a database of fundamental physics experiments. Secondly, in vitro cultured human-derived skin fibroblast HFF-1 cells are treated in three treatment modes of multipolar RF. Cell proliferation, cell activity, and collagen secretion are quantified in the cell biology experiments. Finally, rat dorsal skin is treated to study the effect of different electrode polarity arrangement modes on collagen secretion and skin pathological safety in animal experiments.
The simulation results show that in the case of mode 2, the average values of current density and the uniformity of energy distribution of multipolar RF are better than the other two modes. These results also apply to the mean values of temperature and uniformity of temperature distribution for multipolar RF applied to skin tissue. For the in vitro cell experiments, the number and cell viability of fibroblast HFF-1 cells are effectively increased in all treatment modes of multipolar RF. More importantly, however, the total collagen secretion induced by fibroblast HFF-1 cells is increased by about 10% in mode 2 only, suggesting that RF energy distribution and thermal distribution uniformity may be important parameters for inducing collagen secretion by cells. In animal experiments, the average thickness of the collagen layer of rat skin increase by approximately 0.02, 0.13 and 0.06 mm for the three electrode polarity arrangement modes, respectively. In addition, the pathological safety of rat skin is not affected in any of them.
The following conclusions can be drawn from the simulation and experimental results: (1)The mean current density, energy distribution uniformity and heat distribution uniformity of multipolar RF acting on skin tissue are relatively optimal at the staggered arrangement of positive and negative electrodes. (2) Multipolar RF treatment can effectively promote the proliferation of skin fibroblasts HFF-1 cells cultured in vitro and enhance cell viability, and the application effect is positively correlated with the uniformity of RF energy distribution. (3) The amount of collagen secreted by fibroblasts and the thickness of rat skin collagen layer increase significantly with the increasing uniformity of RF energy distribution. The treatment process of multipolar RF does not affect the pathological safety of the rat skin.
keywords:Multipolar radio frequency, energy distribution, heat distribution, collagen, constant power
DOI: 10.19595/j.cnki.1000-6753.tces.L10090
中图分类号:TM15
国家自然科学基金(52107162)、陕西省科技发展计划(2022CGBX-12, 2022KXJ-57)、中央高校基本科研业务费专项资金(QTZX23064)资助项目。
收稿日期 2023-01-08
改稿日期 2023-05-10
徐 晗男,1995年生,副教授,硕士生导师,研究方向为等离子体物理、等离子体电磁控制、等离子体应用等。E-mail:hxu@xidian.edu.cn
邵明绪男,1988年生,正高级工程师,硕士生导师,研究方向为等离子体技术及应用、射频电磁波热效应及应用等。E-mail:mxshao@xidian.edu.cn(通信作者)
(编辑 郭丽军)