 、HO2、O3及OH在水溶液中的渗透深度分布,并阐释了相关机理。研究表明,氧含量对活性粒子的生成与消耗反应产生较大影响,进而影响到活性粒子在水溶液中的渗透深度。随着氧含量的增加,H2O2、
、HO2、O3及OH在水溶液中的渗透深度分布,并阐释了相关机理。研究表明,氧含量对活性粒子的生成与消耗反应产生较大影响,进而影响到活性粒子在水溶液中的渗透深度。随着氧含量的增加,H2O2、 和HO2的渗透深度减小,但仍维持在数百微米以上的可观量值,而O3和OH的渗透深度增加,并可达20 μm以上,这一深度使得两种粒子可以直接作用到某些生物组织,因而对于等离子体的生物医学应用具有重要意义。
和HO2的渗透深度减小,但仍维持在数百微米以上的可观量值,而O3和OH的渗透深度增加,并可达20 μm以上,这一深度使得两种粒子可以直接作用到某些生物组织,因而对于等离子体的生物医学应用具有重要意义。摘要 大气压低温等离子体作用于生物组织要穿过其表面几十到几百微米厚的水溶液,将会涉及等离子体中活性粒子在水溶液中的传质,而活性粒子的生成与放电气体的氧含量密切相关。该文基于一维流体模型,研究了在放电气体中不同的氧含量下(体积分数为0.1%~5%)大气压He/O2等离子体中五种主要活性粒子H2O2、 、HO2、O3及OH在水溶液中的渗透深度分布,并阐释了相关机理。研究表明,氧含量对活性粒子的生成与消耗反应产生较大影响,进而影响到活性粒子在水溶液中的渗透深度。随着氧含量的增加,H2O2、
、HO2、O3及OH在水溶液中的渗透深度分布,并阐释了相关机理。研究表明,氧含量对活性粒子的生成与消耗反应产生较大影响,进而影响到活性粒子在水溶液中的渗透深度。随着氧含量的增加,H2O2、 和HO2的渗透深度减小,但仍维持在数百微米以上的可观量值,而O3和OH的渗透深度增加,并可达20 μm以上,这一深度使得两种粒子可以直接作用到某些生物组织,因而对于等离子体的生物医学应用具有重要意义。
和HO2的渗透深度减小,但仍维持在数百微米以上的可观量值,而O3和OH的渗透深度增加,并可达20 μm以上,这一深度使得两种粒子可以直接作用到某些生物组织,因而对于等离子体的生物医学应用具有重要意义。
关键词:等离子体粒子传质 氦氧气体 氧含量效应 一维流体模型 等离子体生物医学
近年来,大气压低温等离子体技术快速发展,并且由于其高反应活性、低能耗、环境友好及不需要真空系统等优点,已在生物医学[1]、材料处理[2]、环境保护[3]等多个领域广泛应用。越来越多的研究表明,大气压低温等离子体在生物医学上的应用已呈现出非常显著的效果,如在伤口愈合[4]、杀菌消毒[5]、甚至癌症治疗[6]等方面。
在大气压气体放电过程中,载能电子与气体分子相互作用,使气体分子发生激发、电离、分解及解离吸附等一系列物理和化学过程,产生大量的活性氧粒子(Reactive Oxygen Species, ROS)和活性氮粒子(Reactive Nitrogen Species, RNS)[7]。ROS主要包括氧原子(O)、羟基自由基(OH)、过氧化氢(H2O2)、臭氧(O3)、超氧阴离子( )等;RNS主要包括一氧化氮(NO)、二氧化氮(NO2)、过氧亚硝酸(ONOOH)等[8-11]。在低温等离子体生物医学应用中,对于预期的生物学效应,这些粒子起着关键的作用。比如有报道认为,OH和
)等;RNS主要包括一氧化氮(NO)、二氧化氮(NO2)、过氧亚硝酸(ONOOH)等[8-11]。在低温等离子体生物医学应用中,对于预期的生物学效应,这些粒子起着关键的作用。比如有报道认为,OH和 具有极强的细胞毒性可以杀死有害细胞[12];NO会使伤口愈合的速度提高30%以上[13];尤其,H2O2在细菌灭活、促进细胞增殖等应用中也起到重要作用[14]。然而,生物组织通常都是处于有水的环境中,这使得等离子体作用到被处理物时必然与水溶液发生相互作用[15];同时研究者发现,等离子体产生的带电粒子和活性粒子与水溶液发生反应能够生成新的活性粒子,以上这些改变了生物组织所处的液相环境进而产生生物学效应[7]。因此,研究等离子体产生的活性粒子在水溶液中的传质,对于等离子体在生物医学领域的应用具有重要意义。
具有极强的细胞毒性可以杀死有害细胞[12];NO会使伤口愈合的速度提高30%以上[13];尤其,H2O2在细菌灭活、促进细胞增殖等应用中也起到重要作用[14]。然而,生物组织通常都是处于有水的环境中,这使得等离子体作用到被处理物时必然与水溶液发生相互作用[15];同时研究者发现,等离子体产生的带电粒子和活性粒子与水溶液发生反应能够生成新的活性粒子,以上这些改变了生物组织所处的液相环境进而产生生物学效应[7]。因此,研究等离子体产生的活性粒子在水溶液中的传质,对于等离子体在生物医学领域的应用具有重要意义。
低温等离子体在水溶液中的传质,常有30多种活性粒子,包括H2O2、H+、NO2、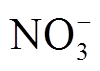 等长寿命粒子,以及OH、
等长寿命粒子,以及OH、 、NO这样的短寿命粒子[16]。这些活性粒子在应用中发挥着多种多样的作用。比如在细菌灭活方面,研究发现,在等离子体直接对细菌悬浮液进行处理时,短寿命粒子如
、NO这样的短寿命粒子[16]。这些活性粒子在应用中发挥着多种多样的作用。比如在细菌灭活方面,研究发现,在等离子体直接对细菌悬浮液进行处理时,短寿命粒子如 、OH等起到了主要的杀菌作用[17];而对于等离子体处理过的水溶液,则是长寿命活性粒子如H2O2、
、OH等起到了主要的杀菌作用[17];而对于等离子体处理过的水溶液,则是长寿命活性粒子如H2O2、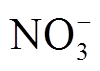 起到杀菌作用[18]。
起到杀菌作用[18]。
在等离子体生物医学应用中,活性粒子在生物组织中的渗透深度是一个关键参数,它决定了活性粒子最终是否能够作用到被处理物,从而完成拟进行的治疗。例如,黑色素瘤一般存在于真皮层中,活性粒子需要穿越200 μm以上的皮肤组织才能起到作用[14]。因此,提高活性粒子在水溶液中的渗透深度十分重要。
目前,已有研究报道了通过调节电子能量来改变五种主要活性粒子OH、H2O2、O3、HO2和 在传质中的渗透深度[19],该研究在氧气体积分数为1%的氦氧工作气体中进行。研究发现,随着电子能量增大,HO2变成短寿命粒子,O3和OH的渗透深度增大,最大能达到几十微米。另有研究表明,应用中使用的等离子体作用效果与活性粒子的粒子数密度和通量密切相关,而活性粒子的粒子数密度和通量则受工作气体成分的影响[20]。另一方面,工作气体(He或Ar)中添加一定体积分数的O2是放电等离子体中产生含氧活性粒子的有效途径。然而,氧含量的变化会在多大程度上影响等离子体与水溶液的相互作用和活性粒子在水溶液中的渗透深度并不清楚。因此,需要探究这些影响,建立氧含量-粒子通量-渗透深度之间的关系,以实现对活性粒子渗透深度的有效调控,为等离子体生物医学应用提供理论参考。
在传质中的渗透深度[19],该研究在氧气体积分数为1%的氦氧工作气体中进行。研究发现,随着电子能量增大,HO2变成短寿命粒子,O3和OH的渗透深度增大,最大能达到几十微米。另有研究表明,应用中使用的等离子体作用效果与活性粒子的粒子数密度和通量密切相关,而活性粒子的粒子数密度和通量则受工作气体成分的影响[20]。另一方面,工作气体(He或Ar)中添加一定体积分数的O2是放电等离子体中产生含氧活性粒子的有效途径。然而,氧含量的变化会在多大程度上影响等离子体与水溶液的相互作用和活性粒子在水溶液中的渗透深度并不清楚。因此,需要探究这些影响,建立氧含量-粒子通量-渗透深度之间的关系,以实现对活性粒子渗透深度的有效调控,为等离子体生物医学应用提供理论参考。
本文基于一维流体模型,研究大气压He/O2等离子体在氧气体积分数为0.1%~5%的范围内,氧气体积分数对OH、H2O2、O3、HO2及 五种重要粒子在水溶液中分布的影响,包括它们的粒子数密度和渗透深度,并通过计算不同粒子的产生与消减对氧含量的依赖,阐释相应的机制。
五种重要粒子在水溶液中分布的影响,包括它们的粒子数密度和渗透深度,并通过计算不同粒子的产生与消减对氧含量的依赖,阐释相应的机制。
本文模拟中,气相区活性粒子的产生模型来自文献[21-22],如图1所示。放电在两个平行的金属板电极之间产生,板间间隙为2 mm;外加射频正弦交流电源,电压幅值为511 V,频率为13.56 MHz,功率密度维持在40 W/cm3;工作气体为氦氧混合气体,气体流速为1 L/min;样品放置在一个板电极上接受等离子体辐照。这些参数的选择已在文献[22]中通过实验得到了验证。
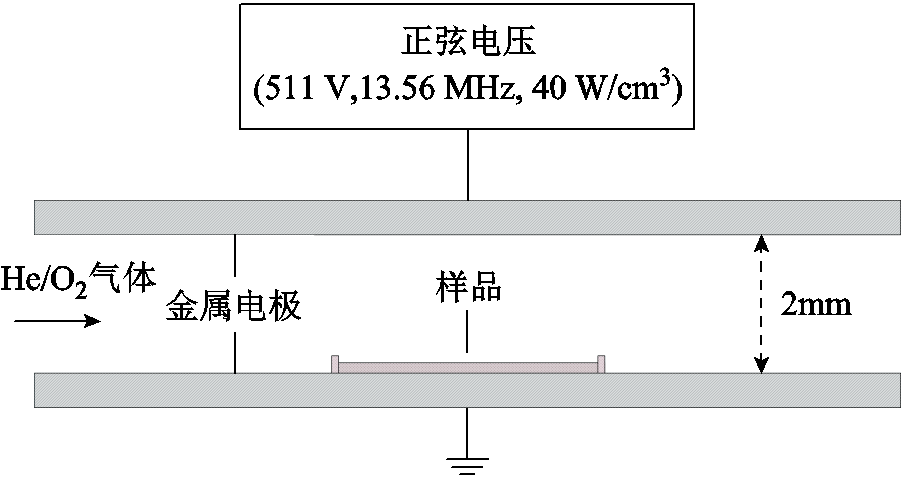
图1 等离子体产生模型
Fig.1 Plasma generation model
为了降低射频放电气体温度过高导致液体蒸发的影响,本模型选取α放电模式使得放电气体温度较低,接近室温300 K[23]。而在实验中也可采取降温措施,如使用循环水冷系统使得气体温度控制在300 K左右[22]。
等离子体进入水溶液的传质过程包括三个区域,如图2所示,即气相等离子体产生区域(气相区)、气液交界区和液相区。目前,由于理论知识的发展仍处于初级阶段,因此对于气相区和液相区分别进行建模,对于气液交界区,则采用压力平衡、离子水合和脱水的瞬时传质假设来进行处理。由于水层的存在,不仅影响活性粒子的迁移,而且在气相区活性粒子的产生和传质中也起着重要作用[24]。因此,对于气相区进入气液交界区和液相区的粒子进行单独分析,是对现实中等离子体实验的粗略近似[25]。
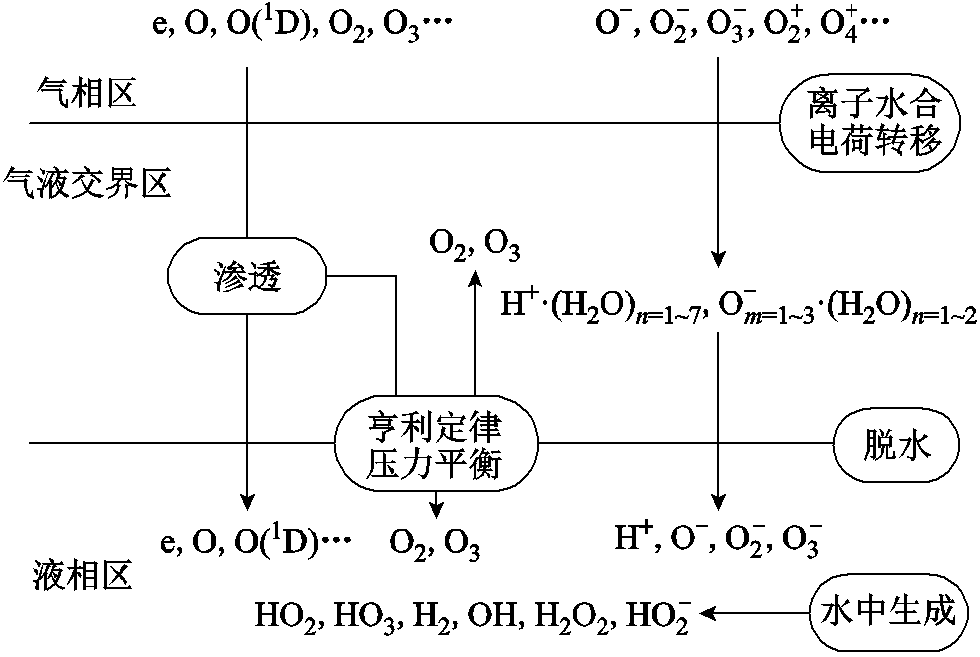
图2 等离子体从气相区到液相区传质示意图
Fig.2 Schematic diagram of the mass transfer processes of the plasmas from the gas region to the liquid region
在气相区,使用一维流体模型来模拟等离子体的产生和传质。由于气液交界区和液相区的水蒸气扩散干扰很小,所以对于气相区的研究需要单独进行。本文研究中,对于工作气体He/O2,考虑的氧气体积分数范围为0.1%~5%,并且主要关注其中五种含氧粒子和电子,即O、O(1D)、O2(a)、 、O3和e。来自气相区产生的等离子体成分的壁通量取自文献[26],该壁通量也是在氦氧气体放电且温度为300 K的条件下计算得到的,以保证和本文设定的条件一致。假定等离子体粒子离开气相区的壁通量没有损失,且除以上六种粒子外的其他粒子不受氧气体积分数变化的影响。表1给出了不同氧气体积分数下,六种粒子进入液相区时的通量(此后简称通量)。
、O3和e。来自气相区产生的等离子体成分的壁通量取自文献[26],该壁通量也是在氦氧气体放电且温度为300 K的条件下计算得到的,以保证和本文设定的条件一致。假定等离子体粒子离开气相区的壁通量没有损失,且除以上六种粒子外的其他粒子不受氧气体积分数变化的影响。表1给出了不同氧气体积分数下,六种粒子进入液相区时的通量(此后简称通量)。
表1 不同氧气体积分数下相关粒子进入液相区的通量
Tab.1 Fluxes of related species before going into the liquid phase at different oxygen concentrations
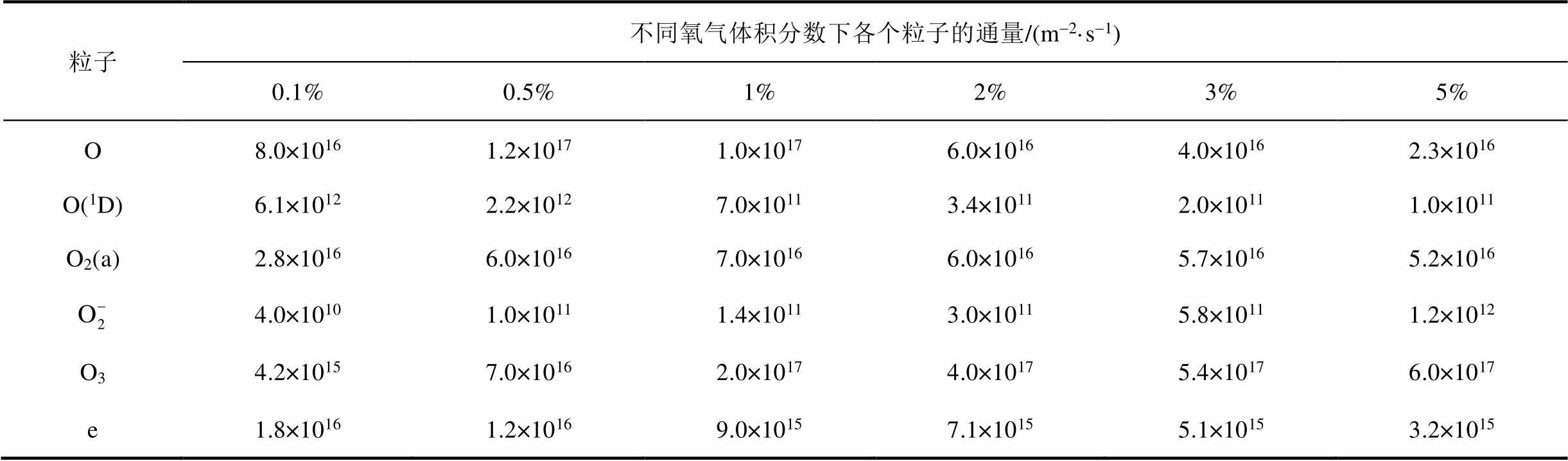
粒子不同氧气体积分数下各个粒子的通量/(m-2·s-1) 0.1%0.5%1%2%3%5% O8.0×10161.2×10171.0×10176.0×10164.0×10162.3×1016 O(1D)6.1×10122.2×10127.0×10113.4×10112.0×10111.0×1011 O2(a)2.8×10166.0×10167.0×10166.0×10165.7×10165.2×1016 4.0×10101.0×10111.4×10113.0×10115.8×10111.2×1012 O34.2×10157.0×10162.0×10174.0×10175.4×10176.0×1017 e1.8×10161.2×10169.0×10157.1×10155.1×10153.2×1015
由于相关粒子传质的时间尺度都在ns量级,因此可以近似地认为气液边界区的传质是一个瞬时过程。ns量级的时间尺度不会涉及相当剧烈的电子反应,且电子在液相区溶剂化很快,只有几十皮秒,因此也可以假设电子通过气液交界区时没有损耗,通量不变[19]。根据这一假设,穿过气相区的大多数粒子可以最大程度地保持其通量。对于少部分粒子则需要考虑一些理化反应,比如O3,该粒子穿越气相区时需要满足亨利定律。而对于一些离子,比如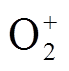 、O4+、O-、
、O4+、O-、 与
与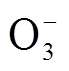 ,刚接触气液边界时马上就要和水蒸气发生电荷转移反应生成水合离子;在进入液相区后,水合离子经过快速脱水释放出H+、O-和
,刚接触气液边界时马上就要和水蒸气发生电荷转移反应生成水合离子;在进入液相区后,水合离子经过快速脱水释放出H+、O-和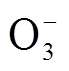 等离子,在此基础上,通过电荷守恒定律可得到这些离子进入液相区时的通量。
等离子,在此基础上,通过电荷守恒定律可得到这些离子进入液相区时的通量。
所以,在已知气相区的壁通量的基础上,根据气液交界区瞬时传质假设,表2给出了进入液相区的19种粒子的通量,作为下一阶段液相区中反应物传质的边界条件。本文将液相区深度设置为10 mm,该深度远大于生物膜的典型厚度,因此在模拟中可将液相区深度视为无穷大。
表2 相关粒子进入液相区的通量及扩散系数
Tab.2 Flux and diffusion coefficient of related particles going into the liquid phase
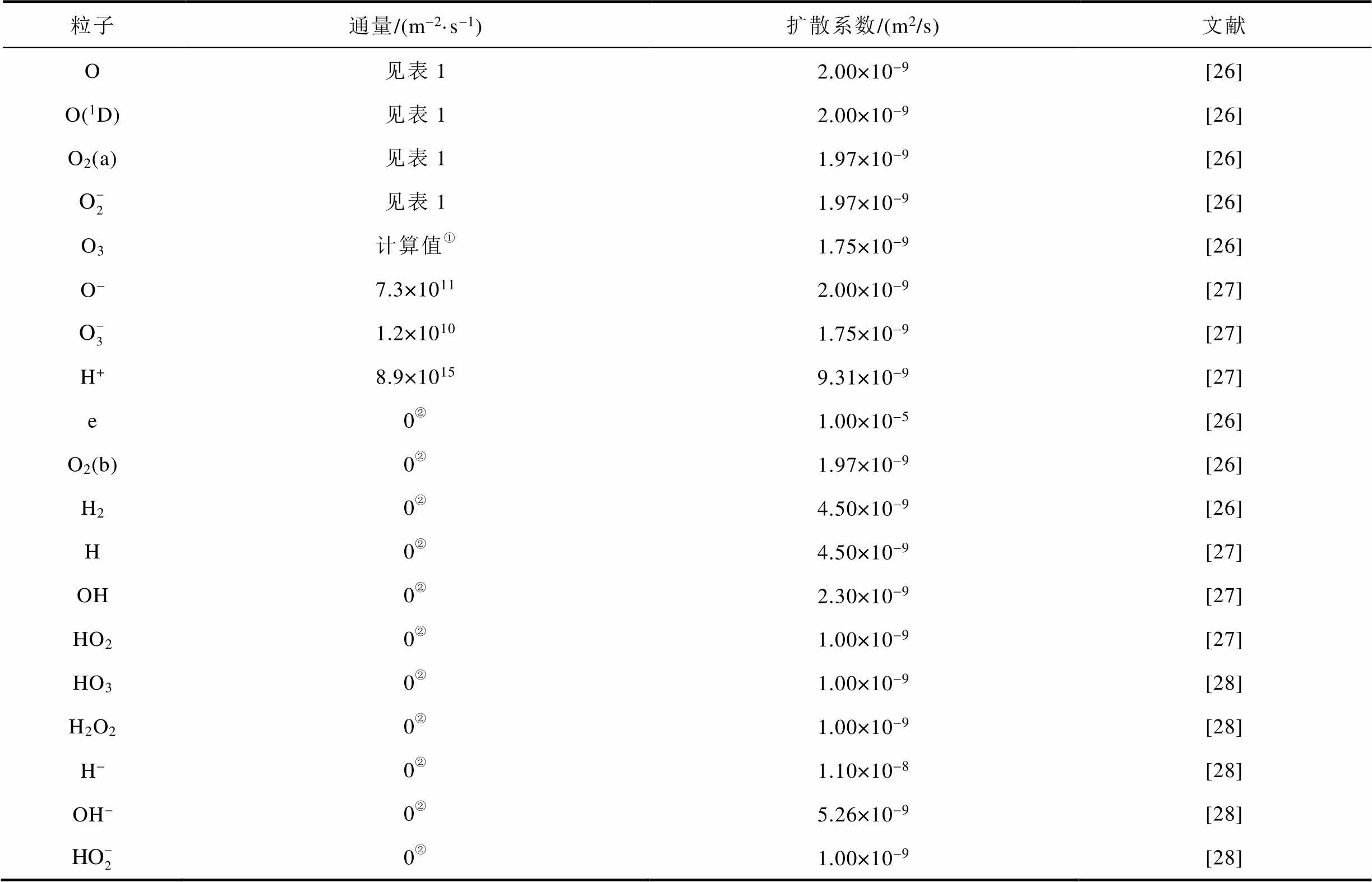
粒子通量/(m-2·s-1)扩散系数/(m2/s)文献 O见表12.00×10-9[26] O(1D)见表12.00×10-9[26] O2(a)见表11.97×10-9[26] 见表11.97×10-9[26] O3计算值①1.75×10-9[26] O-7.3×10112.00×10-9[27] 1.2×10101.75×10-9[27] H+8.9×10159.31×10-9[27] e0②1.00×10-5[26] O2(b)0②1.97×10-9[26] H20②4.50×10-9[26] H0②4.50×10-9[27] OH0②2.30×10-9[27] HO20②1.00×10-9[27] HO30②1.00×10-9[28] H2O20②1.00×10-9[28] H-0②1.10×10-8[28] OH-0②5.26×10-9[28] 0②1.00×10-9[28]
①计算O3进入液相的通量时需应用亨利定律,亨利系数取0.3。
②所涉及的粒子仅在液相区中产生,故通量设置为0。
液相区考虑的粒子及其之间的化学反应取自已发表的等离子体与水溶液相互作用的研究,共计19种粒子和84个反应,具体所发生的化学反应及相应的反应速率系数见表3。表中反应速率系数单位中的M代表mol/L,单体反应速率单位取为s-1,二体反应速率单位取为M-1·s-1。由于进入到液相区的电子动能比气相区小得多,因此本文未考虑高能电子在水溶液中的反应。
表3 液相区的化学反应及相应的反应速率系数
Tab.3 Chemical reactions and the corresponding rate coefficients in the liquid region
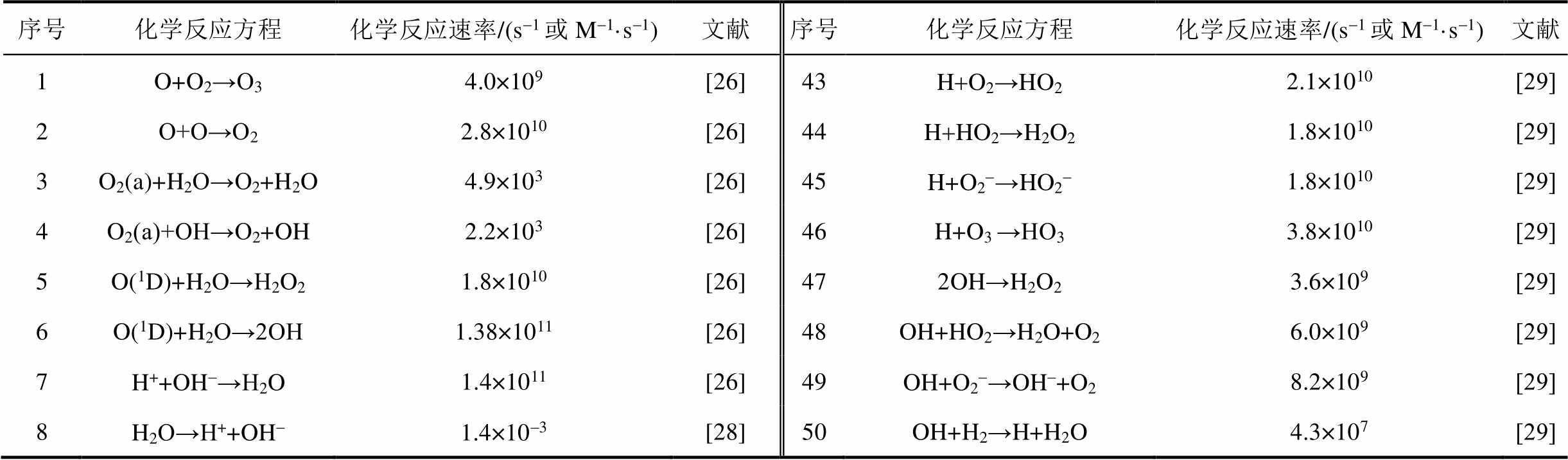
序号化学反应方程化学反应速率/(s-1或M-1·s-1)文献序号化学反应方程化学反应速率/(s-1或M-1·s-1)文献 1O+O2→O34.0×109[26]43H+O2→HO22.1×1010[29] 2O+O→O22.8×1010[26]44H+HO2→H2O21.8×1010[29] 3O2(a)+H2O→O2+H2O4.9×103[26]45H+O2-→HO2-1.8×1010[29] 4O2(a)+OH→O2+OH2.2×103[26]46H+O3 →HO33.8×1010[29] 5O(1D)+H2O→H2O21.8×1010[26]472OH→H2O23.6×109[29] 6O(1D)+H2O→2OH1.38×1011[26]48OH+HO2→H2O+O26.0×109[29] 7H++OH-→H2O1.4×1011[26]49OH+O2-→OH-+O28.2×109[29] 8H2O→H++OH-1.4×10-3[28]50OH+H2→H+H2O4.3×107[29]
(续)

序号化学反应方程化学反应速率/(s-1或M-1·s-1)文献序号化学反应方程化学反应速率/(s-1或M-1·s-1)文献 9H2O2→H++HO2-1.12×10-1[28]51OH+H2O2→HO2+H2O2.7×107[29] 10H++HO2-→H2O25.0×1010[28]52OH+O-→HO2-2.5×1010[29] 11H2O2+OH-→HO2-+H2O1.3×1010[28]53OH+HO2-→HO2+OH-7.5×109[29] 12HO2-+H2O→H2O2+OH-5.8×107[28]54OH+O3-→O3+OH-2.6×109[29] 13e+H2O→H+OH-1.9×101[28]55OH+O3-→2O2-+H+6.0×109[29] 14H+OH-→e+H2O2.2×107[28]56OH+O3→HO2+O21.1×108[29] 15H→e +H+3.9[29]57HO2+O2-→HO2-+O28.0×107[29] 16e+H+→H2.3×1010[29]58HO2+HO2→H2O2+O27.0×105[29] 17OH+OH-→O-+H2O1.3×1010[29]59HO2+O-→O2+OH-6.0×109[29] 18O-+H2O→OH +OH-1.03×108[29]60HO2+H2O2→OH+O2+H2O5.0×10-1[29] 19OH→O-+H+1.26×10-1[29]61HO2+HO2-→OH+O2+OH-5.0×10-1[29] 20O-+H+→OH1.0×1011[29]62HO2+O3-→2O2+OH-6.0×109[29] 21HO2→O2-+H+1.35×106[29]63HO2+O3→HO3+O25.0×108[29] 22O2-+H+→HO25.0×1010[29]642O2-+2H2O→H2O2+O2+2OH-1.0×102/[H2O]2 M-3·s-1[29] 23HO2+OH-→O2-+H2O5.0×1010[29]65O2-+O-+H2O→O2+2OH-6.0×108/[H2O] M-2·s-1[29] 24O2-+H2O→HO2+OH-18.5767[29]66O2-+H2O2→OH+O2+OH-1.3×10-1[29] 25e+OH→OH-3.0×1010[29]67O2-+HO2-→O-+O2+OH-1.3×10-1[29] 26e+H2O2→OH+OH-1.1×1010[29]68O2-+O3-+H2O→2O2+2OH-1.0×104/[H2O] M-2·s-1[29] 27e+O2-+H2O→HO2-+OH-1.3×1010/[H2O] M-2·s-1[29]69O2-+O3→O3-+O21.5×109[29] 28e+HO2→HO2-2.0×1010[29]702O-+H2O→HO2-+OH-1.0×109/[H2O] M-2·s-1[29] 29e+O2→O2-1.9×1010[29]71O-+O2→O3-3.6×109[29] 302e+2H2O→H2+2OH-5.5×109/[H2O]2 M-3·s-1[29]72O-+H2→H+OH-8.0×107[29] 31e+H+H2O →H2+OH-2.5×1010/[H2O] M-2·s-1[29]73O-+H2O2→O2-+H2O5.0×108[29] 32e+HO2-→O-+OH-3.5×1010[29]74O-+HO2-→O2-+OH-4.0×108[29] 33e+O-+H2O→OH-+OH-2.2×1010/[H2O] M-2·s-1[29]75O-+O3-→2O2-7.0×108[29] 34e+O3-+H2O→O2 +2OH-1.6×1010/[H2O] M-2·s-1[29]76O-+O3→O2-+O25.0×109[29] 35e+O3 →O3-3.6×1010[29]77O3-→O2+O-3.3×103[29] 36H+ H2O→H2+OH1.1×101[29]78O3-+H+→O2+OH9.0×1010[29] 37H+O-→OH-1.0×1010[29]79HO3→O2+OH1.1×105[29] 38H+HO2-→OH+OH-9.0×107[29]80O+OH-→HO2-1.1×105[29] 39H+O3-→OH-+O21.0×1010[29]81H2O2+O→OH+HO21.6×105[29] 40H+H →H27.8×109[29]82H2O2→2OH2.3×10-7[29] 41H+OH →H2O7.0×109[29]83O+HO2-→OH+O2-5.3×109[29] 42H+H2O2→OH+H2O9.0×107[29]84O3+H2O2→OH+HO2+O23.0×109[29]
采用一维流体漂移扩散模型对粒子在液相区的分布与行为进行描述,基本控制方程为
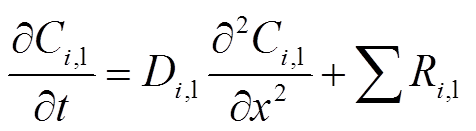 (1)
(1)
式中,下标i和l分别代表粒子种类和液体;Ci,l为i类粒子在液相中的粒子数密度;Di,l为i类粒子相对应的扩散系数(见表2);t为时间;x为粒子在液体中的渗透深度;Ri,l为相应粒子化学反应的反应速率。
液相区的中性粒子通量G可表示为
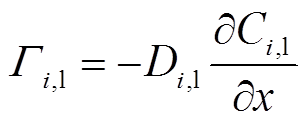 (2)
(2)
由于活性粒子自身水解带来的电场会对带电粒子行为产生不可忽视的影响,因此带电粒子的通量需要单独考虑,可表示为
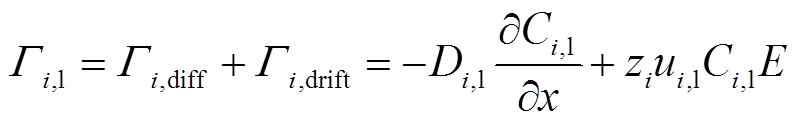 (3)
(3)
式中,Γi,diff为扩散通量;Γi,drift为漂移通量;zi为带电粒子的电荷数;ui,l为带电粒子的迁移率;E为电场强度。电场强度和迁移率可分别通过泊松方程和能斯特-爱因斯坦方程计算得出。
由式(1)~式(3)可以得到
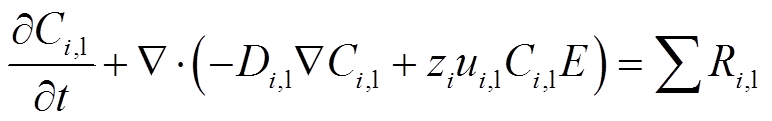 (4)
(4)
由于设置的液相层深度d0=10 mm,x=0即为液相表面,此时刚到达液相区的带电粒子和中性粒子的通量与气相区的通量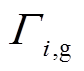 一致。带电粒子仍需考虑自身水解的电场作用,因此其通量可以表示为
一致。带电粒子仍需考虑自身水解的电场作用,因此其通量可以表示为
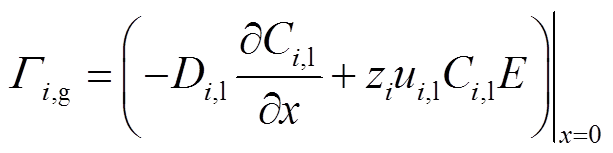 (5)
(5)
此外,除O3以外的中性粒子进入液相区的通量表示为
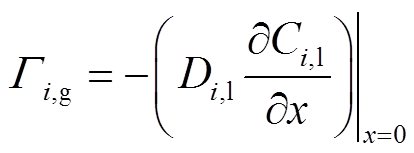 (6)
(6)
而对于特殊的中性粒子O3,考虑到该粒子的粒子数密度过低时无法进入液相区,因此在液相区需满足亨利定律,即
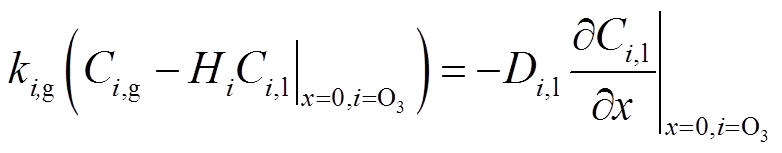 (7)
(7)
式中,Hi为亨利系数;Ci,g为粒子在气相区的粒子数密度,根据文献[26],取O3的气相区粒子数密度为1.5×1015 cm-3;ki,g为粒子在气相区的传输系数,ki,g=Γi,g/Ci,g。
在液相区最底层,即x=d0=10 mm处,假定所有粒子都已经达到稳定状态,即无论是中性粒子还是带电粒子,均满足
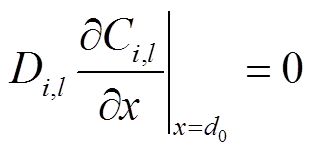 (8)
(8)
当等离子体中活性粒子到达液相区表面时,需要给其粒子数密度设定一个初始值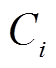 。水溶液的PH值为7,通过换算得
。水溶液的PH值为7,通过换算得 。水的分子数密度可通过密度1 g/mL与摩尔质量18 g/mol的关系计算得到
。水的分子数密度可通过密度1 g/mL与摩尔质量18 g/mol的关系计算得到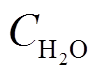 =3.35×1028 m-3。在300 K时,假定O2在水中处于饱和状态,即
=3.35×1028 m-3。在300 K时,假定O2在水中处于饱和状态,即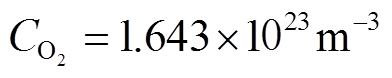 。相对于其他粒子,H2O和O2的分子数密度要高出几个数量级,因此在传质模拟中,将其分子数密度设置为固定值,不受其他反应干扰。其余粒子的粒子数密度初值设置为Ci=1011 m-3。
。相对于其他粒子,H2O和O2的分子数密度要高出几个数量级,因此在传质模拟中,将其分子数密度设置为固定值,不受其他反应干扰。其余粒子的粒子数密度初值设置为Ci=1011 m-3。
基于第1节描述的模型,对等离子体在液相区的传质进行了数值模拟。计算表明,短寿命粒子,如e、H、O和O(1d)等,在进入液相区后主要与其他粒子反应形成更稳定的活性粒子,其中H2O2、O2–、HO2、O3和OH通常被认为是最终可能与被处理物相互作用的粒子[30],因此,这里将主要关注它们在液相区传质中的分布。等离子体处理水溶液60 s后,在不同氧气体积分数下,H2O2、 、HO2、O3和OH在水溶液中的深度分布分别如图3a~图3e所示。计算时发现当五种粒子的粒子数密度为5×1011 cm-3时,五种活性粒子的渗透深度均已基本稳定,该粒子数密度下能够清楚地观察和比较不同粒子的最大渗透深度的差异,因此将粒子数密度阈值取为5×1011 cm-3。
、HO2、O3和OH在水溶液中的深度分布分别如图3a~图3e所示。计算时发现当五种粒子的粒子数密度为5×1011 cm-3时,五种活性粒子的渗透深度均已基本稳定,该粒子数密度下能够清楚地观察和比较不同粒子的最大渗透深度的差异,因此将粒子数密度阈值取为5×1011 cm-3。
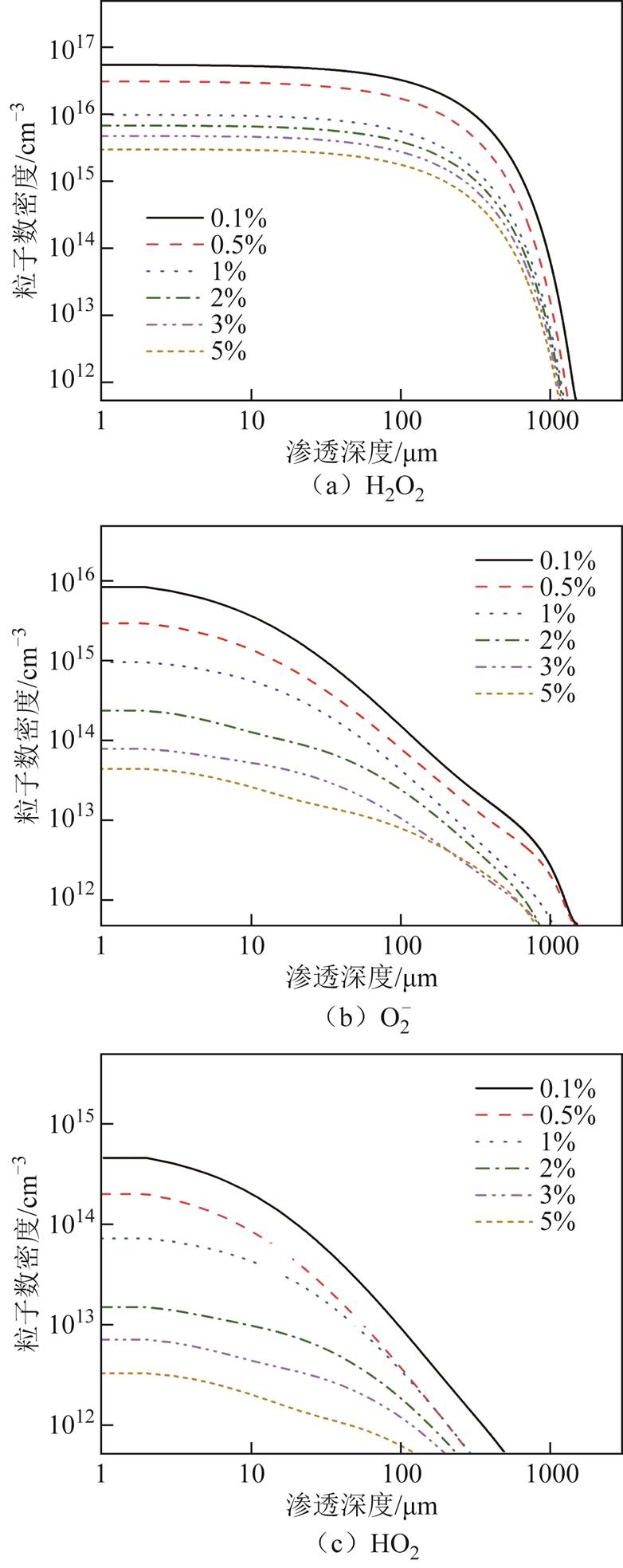
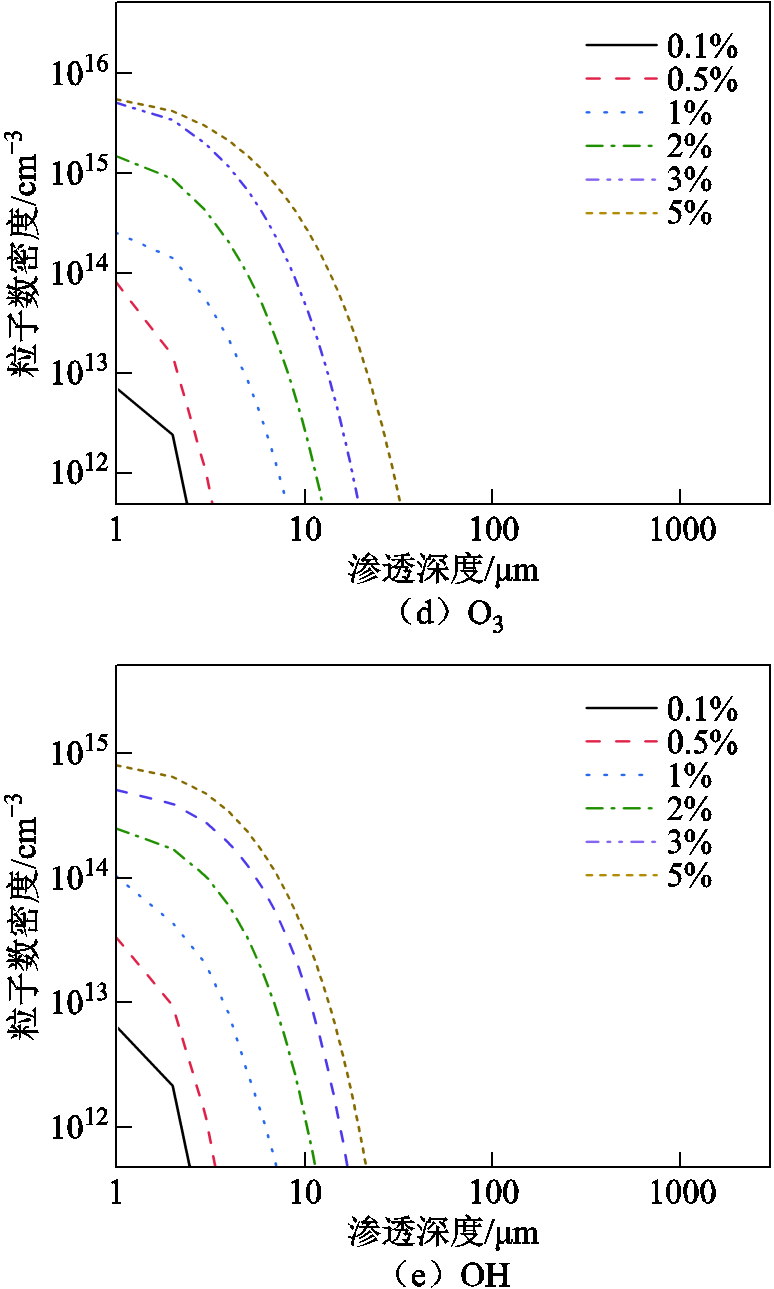
图3 不同氧气体积分数下,五种粒子在水溶液中的深度分布
Fig.3 Depth distributions of five ROSs in aqueous solution at different oxygen volume
由图3a可以看到,对于给定的氧气体积分数,H2O2的粒子数密度在相当一段深度范围内变化很小;但深度一定时,H2O2的粒子数密度随氧含量的增加明显减小,在考虑的氧气体积分数范围内,差异接近两个数量级。此外,也能够观察到,氧含量增大使H2O2的最大渗透深度减小。
对于 (见图3b),不同的氧气体积分数下,在氧气体积分数一定时,
(见图3b),不同的氧气体积分数下,在氧气体积分数一定时, 的粒子数密度均随深度增加平稳下降;而深度一定时,
的粒子数密度均随深度增加平稳下降;而深度一定时, 的粒子数密度随氧含量的增加而降低,且最大渗透深度亦减小。比较图3b和图3c,能够看到氧含量对HO2的影响与对
的粒子数密度随氧含量的增加而降低,且最大渗透深度亦减小。比较图3b和图3c,能够看到氧含量对HO2的影响与对 的类似。
的类似。
图3d和图3e表明,氧含量对O3和OH的影响类似。不同氧气体积分数下,在氧气体积分数一定时,两种粒子的粒子数密度均随深度增加下降;但对于确定的深度,粒子的粒子数密度随氧含量增加而增大,粒子的最大渗透深度增加,这与前三种活性粒子的最大渗透深度对氧含量的依赖相反。
如前文中所提到,活性粒子在水溶液中的渗透深度是一个关键参数。因此,为了能够清楚地表明氧含量对五种活性粒子在水溶液中渗透深度的影响,图4给出了它们的最大渗透深度随氧气体积分数的变化。
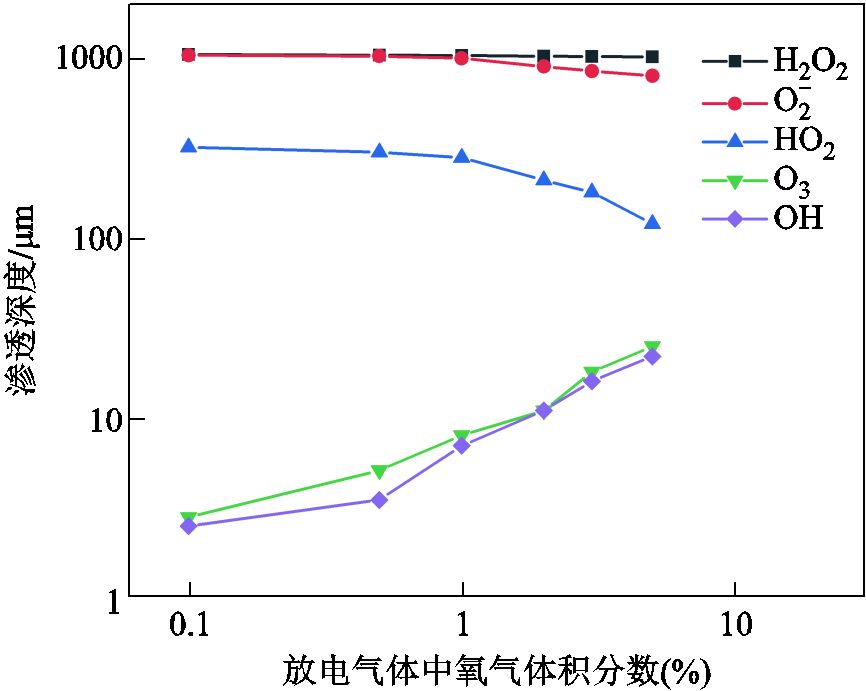
图4 五种活性氧粒子最大渗透深度随氧气体积分数的变化
Fig.4 Maximum depths of five ROSs as a function of oxygen volume fraction
可以看到,在一定的氧气体积分数下,粒子的渗透深度按OH、O3、HO2、 和H2O2的顺序依次增大,但O3和OH的十分接近。此外,随着氧含量的增加,HO2、
和H2O2的顺序依次增大,但O3和OH的十分接近。此外,随着氧含量的增加,HO2、 和H2O2的渗透深度有相对小的减小,而O3和OH的则显著增加。当氧气体积分数从0.1%增加到5%时,HO2的渗透深度从320 μm降低到了120 μm,而H2O2与
和H2O2的渗透深度有相对小的减小,而O3和OH的则显著增加。当氧气体积分数从0.1%增加到5%时,HO2的渗透深度从320 μm降低到了120 μm,而H2O2与 虽然也有减少,但H2O2均在1 000 μm之上,
虽然也有减少,但H2O2均在1 000 μm之上, 相比H2O2降低得更多,但也在800 μm以上。对于O3和OH,它们的渗透深度在氧气体积分数为0.1%时约为2 μm,而当氧气体积分数提高到5%时可达20 μm以上。
相比H2O2降低得更多,但也在800 μm以上。对于O3和OH,它们的渗透深度在氧气体积分数为0.1%时约为2 μm,而当氧气体积分数提高到5%时可达20 μm以上。
图4的结果表明,增大氧含量后,尽管HO2、 和H2O2的最大渗透深度减小,但仍保持在一个可观的量值上;而另一方面,O3和OH的最大渗透深度能够增大到20 μm以上。这一渗透深度具有重要的意义,尤其是对于OH,其氧化电位达到2.8 V,对于细胞来说具有极大的毒性[12];此外,OH对DNA的抽氢作用能够让DNA链断裂[31]。因此,可以通过提高氧含量来显著增加OH的渗透深度,从而在等离子体生物医学应用中能够更有效地利用OH的生物学作用。
和H2O2的最大渗透深度减小,但仍保持在一个可观的量值上;而另一方面,O3和OH的最大渗透深度能够增大到20 μm以上。这一渗透深度具有重要的意义,尤其是对于OH,其氧化电位达到2.8 V,对于细胞来说具有极大的毒性[12];此外,OH对DNA的抽氢作用能够让DNA链断裂[31]。因此,可以通过提高氧含量来显著增加OH的渗透深度,从而在等离子体生物医学应用中能够更有效地利用OH的生物学作用。
至此,能够看到工作气体中氧含量对上述五种粒子在水溶液中粒子数密度分布的显著影响。接下来将通过对生成和消减这五种粒子的主要反应进行定量分析来阐释其机制,即对每一种粒子,计算其在不同氧气体积分数下的生成量、消减量和净生成量。需要指出,当氧气体积分数一定时,这些粒子的粒子数密度随渗透深度分布的机制已在文献[19]中阐释。另一方面,在图3中已表明,在粒子的整个渗透深度范围内,五种粒子的粒子数密度变化随氧含量的增加均呈现单一的增加(O3、OH)或减少(H2O2、 、HO2)。因此,以下对这种现象进行分析,并以粒子渗透初始阶段的分布加以阐释。
、HO2)。因此,以下对这种现象进行分析,并以粒子渗透初始阶段的分布加以阐释。
1)H2O2
H2O2的主要生成反应有O(1D)+H2O→H2O2、H2O+ →H2O2+OH-和
→H2O2+OH-和 +H+→H2O2,而主要的消减反应包括OH+H2O2→HO2+H2O及O3+H2O2→ OH+HO2+O2。如表1所示,随着氧含量的增大,O(1D)的通量减小,因此O(1D)+H2O→H2O2所生成的H2O2减少,在考虑的氧气体积分数范围中,随着氧含量的增加,H2O2生成量从7.124×1018 cm-3下降到1.668×1017 cm-3。同样从表1能够看到,电子的通量随氧含量增大而减小,而通过一系列与电子相关的反应可使
+H+→H2O2,而主要的消减反应包括OH+H2O2→HO2+H2O及O3+H2O2→ OH+HO2+O2。如表1所示,随着氧含量的增大,O(1D)的通量减小,因此O(1D)+H2O→H2O2所生成的H2O2减少,在考虑的氧气体积分数范围中,随着氧含量的增加,H2O2生成量从7.124×1018 cm-3下降到1.668×1017 cm-3。同样从表1能够看到,电子的通量随氧含量增大而减小,而通过一系列与电子相关的反应可使 的生成量减少[21],因此反应
的生成量减少[21],因此反应  +H2O→ H2O2+OH-和
+H2O→ H2O2+OH-和 +H+→H2O2对H2O2的生成量均减小,分别从2.46×1018 cm-3和4.6×1017 cm-3降低到9.64×1016 cm-3和3.68×1016 cm-3。上述结果表明,H2O2的总生成量随氧含量增加而减小,且生成量在液相区深处与
+H+→H2O2对H2O2的生成量均减小,分别从2.46×1018 cm-3和4.6×1017 cm-3降低到9.64×1016 cm-3和3.68×1016 cm-3。上述结果表明,H2O2的总生成量随氧含量增加而减小,且生成量在液相区深处与 有关。此外,能够观察到,H2O2的粒子数密度在约500 μm处急速下降。这是因为
有关。此外,能够观察到,H2O2的粒子数密度在约500 μm处急速下降。这是因为 主要由O2-与HO2反应生成,根据图3b和图3c,
主要由O2-与HO2反应生成,根据图3b和图3c, 与HO2在约500 μm处的粒子数密度已降到很小,故
与HO2在约500 μm处的粒子数密度已降到很小,故 生成量急剧减少,这就导致了H2O2粒子数密度的快速下降。
生成量急剧减少,这就导致了H2O2粒子数密度的快速下降。
H2O2的主要消减反应包括H2O2+OH→HO2+H2O和H2O2+O3→OH+HO2+O2,二者引起的H2O2消减均随氧含量增大而增大,消减量分别从8.236×1012 cm-3和3.382×1013 cm-3上升到3.62×1014 cm-3和1.568×1015 cm-3。这种变化可归结到O3和OH均随氧含量增大而增大(见之后的分析)。
H2O2的总生成量、总消减量及净生成量随氧气体积分数的变化如图5所示。可以看到,总生成量远大于总消减量,但差异随氧含量增加而逐渐减小,净生成量也随氧含量增加而减小,从而呈现了图3a所示的H2O2的粒子数密度随氧含量增加而减小的这一依赖。
2)
不同氧气体积分数下,单位时间内 总生成量、总消减量和总净生成量如图6所示。
总生成量、总消减量和总净生成量如图6所示。 的主要生成反应包括HO2→
的主要生成反应包括HO2→ +H+和e+O2→
+H+和e+O2→ 。计算表明,不同氧气体积分数下,HO2→
。计算表明,不同氧气体积分数下,HO2→ +H+对
+H+对 生成的贡献均占主导地位,生成量随氧含量的增加而减小,从2.005×1018 cm-3下降到6.124×1016 cm-3。另一方面,反应
生成的贡献均占主导地位,生成量随氧含量的增加而减小,从2.005×1018 cm-3下降到6.124×1016 cm-3。另一方面,反应 +H+→HO2对O2-消减的贡献起主导作用,消减量随氧含量的增加而减小,从2.01×1018 cm-3下降到6.224×1016 cm-3。以上结果表明,氧含量一定时,HO2→
+H+→HO2对O2-消减的贡献起主导作用,消减量随氧含量的增加而减小,从2.01×1018 cm-3下降到6.224×1016 cm-3。以上结果表明,氧含量一定时,HO2→ +H+生成的
+H+生成的 粒子数量与
粒子数量与 +H+→HO2消耗的
+H+→HO2消耗的 粒子数量几乎相同,因此,反应e+O2→
粒子数量几乎相同,因此,反应e+O2→ 成为
成为 生成的主要来源。如表1所示,随着氧含量的增大,电子的通量减小,因此,
生成的主要来源。如表1所示,随着氧含量的增大,电子的通量减小,因此, 的生成量随氧含量的增加而减小,从6.85×1017 cm-3下降到7.72×1015 cm-3。
的生成量随氧含量的增加而减小,从6.85×1017 cm-3下降到7.72×1015 cm-3。
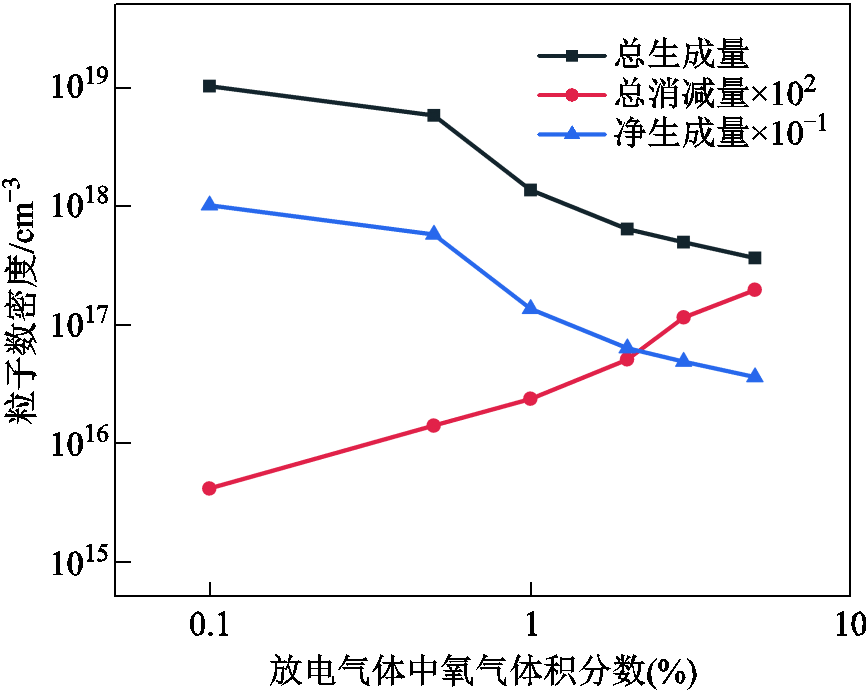
图5 不同氧气体积分数下,单位时间内H2O2总生成量、总消减量和总净生成量
Fig.5 Total generated quantity, total consumption quantity, and total net generation quantity of H2O2 in unit time as a function of oxygen volume fration
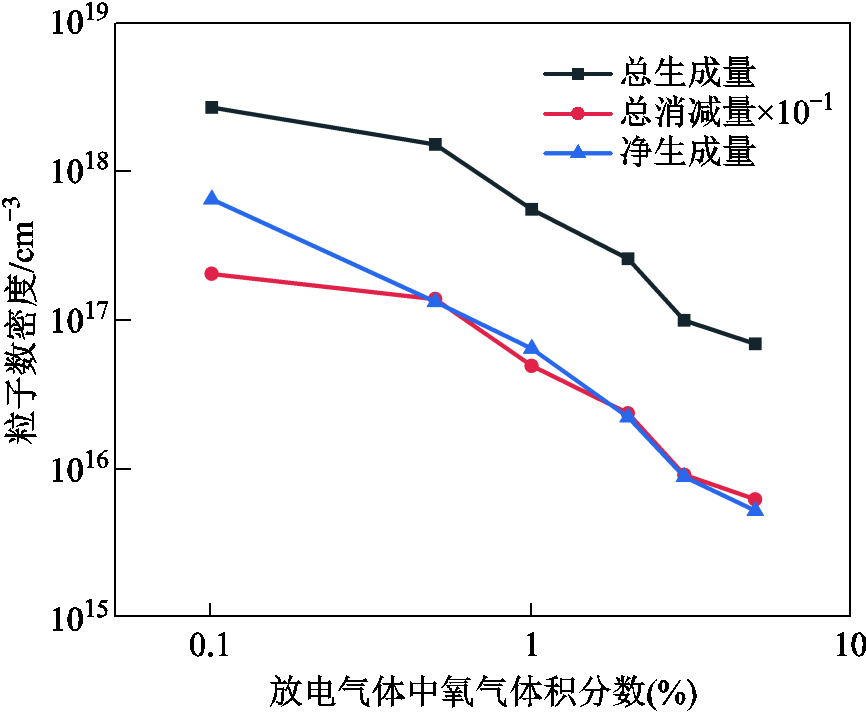
图6 不同氧气体积分数下,单位时间内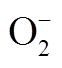 总生成量、总消减量和总净生成量
总生成量、总消减量和总净生成量
Fig.6 Total generation quantity, total consumption quantity, and total net generation quantity of 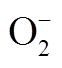 in unit time as a function of oxygen volume fraction
in unit time as a function of oxygen volume fraction
在 的消减反应中,除了
的消减反应中,除了 +H+→HO2之外,主要还有OH+
+H+→HO2之外,主要还有OH+ →OH-+O2和
→OH-+O2和 +O3→
+O3→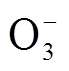 +O2。注意到在表1中,
+O2。注意到在表1中, 的通量随氧气体积分数的增大而增大,且O3和OH的粒子数密度也随氧含量增大而增大(见图3d和图3e初始阶段O3和OH随氧气体积分数的变化),所以这两个反应的
的通量随氧气体积分数的增大而增大,且O3和OH的粒子数密度也随氧含量增大而增大(见图3d和图3e初始阶段O3和OH随氧气体积分数的变化),所以这两个反应的 的消减量随氧含量增大而增大,分别从7.35×1013 cm-3和1.482×1014 cm-3上升到3.46×1014 cm-3和2.542×1015 cm-3。尽管如此,与
的消减量随氧含量增大而增大,分别从7.35×1013 cm-3和1.482×1014 cm-3上升到3.46×1014 cm-3和2.542×1015 cm-3。尽管如此,与 +H+→HO2对
+H+→HO2对 的消减相比,上述两个反应带来的消减量的数量级明显较小,因此
的消减相比,上述两个反应带来的消减量的数量级明显较小,因此 的总消减量随氧含量增大而减小。
的总消减量随氧含量增大而减小。
综上所述,如图6所示,随着氧含量的增大, 的生成量和消减量均减少,
的生成量和消减量均减少, 的净生成量减小,因而在水溶液中
的净生成量减小,因而在水溶液中 的粒子数密度呈现了图3b表明的随氧含量增大而减少。该计算结果与文献[32]中的实验观察一致。
的粒子数密度呈现了图3b表明的随氧含量增大而减少。该计算结果与文献[32]中的实验观察一致。
3)HO2
不同氧气体积分数下,单位时间内HO2总生成量、总消减量和总净生成量如图7所示。HO2主要通过反应 +H+→HO2生成,计算结果表明,HO2生成量随氧含量增加而减小,这与
+H+→HO2生成,计算结果表明,HO2生成量随氧含量增加而减小,这与 的含量随氧含量增加而减小一致。HO2的消减反应除了HO2→
的含量随氧含量增加而减小一致。HO2的消减反应除了HO2→ +H+外,还包括HO2+
+H+外,还包括HO2+ →
→ +O2、OH+HO2→ H2O+O2和HO2+O3→HO3+O2。随着氧含量的增大,HO2+
+O2、OH+HO2→ H2O+O2和HO2+O3→HO3+O2。随着氧含量的增大,HO2+ →
→ +O2所引起的HO2消减减少,消减量从1.32×1013 cm-3下降到4.84×1011 cm-3,但OH+HO2→H2O+O2和O3+HO2→HO3+O2所引起的HO2的消减增大,分别从1.26×1012 cm-3和8.16×1011 cm-3上升到8.32×1013cm-3和4.56×1013cm-3。这些变化可以归因于随着氧含量的增大,
+O2所引起的HO2消减减少,消减量从1.32×1013 cm-3下降到4.84×1011 cm-3,但OH+HO2→H2O+O2和O3+HO2→HO3+O2所引起的HO2的消减增大,分别从1.26×1012 cm-3和8.16×1011 cm-3上升到8.32×1013cm-3和4.56×1013cm-3。这些变化可以归因于随着氧含量的增大, 粒子数密度减少,O3和OH粒子数密度增大。
粒子数密度减少,O3和OH粒子数密度增大。
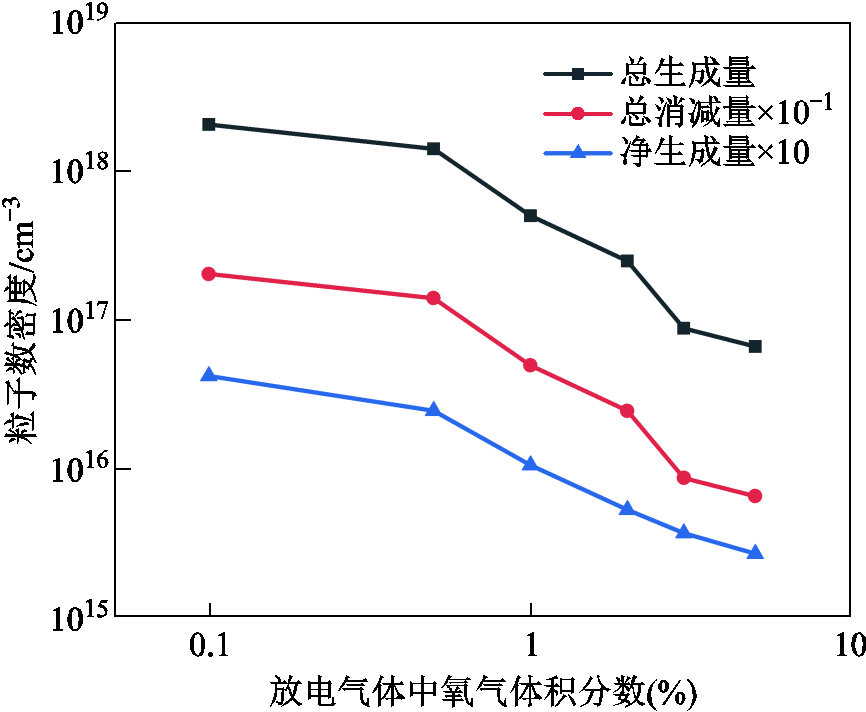
图7 不同氧气体积分数下,单位时间内HO2总生成量、总消减量和总净生成量
Fig.7 Total generation quantity, total consumption quantity, and total net generation quantity of HO2 in unit time as a function of oxygen volume fraction
而在之前对于 的分析中表明,随着氧含量的增大,HO2→
的分析中表明,随着氧含量的增大,HO2→ +H+对于
+H+对于 的生成和
的生成和 +H+→HO2对于
+H+→HO2对于 的消减相当,因而同样意味着两种反应对HO2的消减和生成相当。因此,由于反应HO2+
的消减相当,因而同样意味着两种反应对HO2的消减和生成相当。因此,由于反应HO2+ →
→ +O2、OH+HO2→H2O+O2和HO2+O3→HO3+O2对HO2消减的贡献,在量级上明显小于HO2→
+O2、OH+HO2→H2O+O2和HO2+O3→HO3+O2对HO2消减的贡献,在量级上明显小于HO2→ +H+对于HO2的消减,所以HO2的总生成量比总消减量要大,从而净生成量随氧含量的增加而减小,如图7所示。这一结果导致了图3c所示的HO2粒子数密度随氧含量增大而明显减小。
+H+对于HO2的消减,所以HO2的总生成量比总消减量要大,从而净生成量随氧含量的增加而减小,如图7所示。这一结果导致了图3c所示的HO2粒子数密度随氧含量增大而明显减小。
4)O3
O3的生成主要由反应O+O2→O3以及由气相区进入液相区的O3两部分贡献构成。气体放电产生的O(见表1)在刚进入液相区即与水中大量的O2通过反应O+O2→O3生成O3。经计算得到,反应O+O2→O3在氧气体积分数为0.5%时,得到的O3生成量最大,为8.64×1014 cm-3,与表1中O的通量在氧气体积分数为0.5%时为最大相符合。液相区中来自于气相区的O3的溶解量随氧含量增大而增大,且也在刚进入液相区时粒子数密度达到最大,从1.16×1014 cm-3上升到1.502×1016 cm-3,这与表1中O3的通量随氧含量增大而增大的现象一致。这两种反应在液相区生成的O3的总量随氧含量增加而增加,且集中在粒子刚进入液相区的阶段。
反应O3+ →
→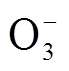 +O2和O3+H2O2→OH+HO2+O2主导了O3的消减。之前的分析表明,
+O2和O3+H2O2→OH+HO2+O2主导了O3的消减。之前的分析表明, 和H2O2的粒子数密度均随氧含量的增大而减小,但在考虑的氧气体积分数范围内,在水溶液中粒子渗透的初始阶段,H2O2的粒子数密度在1015cm-3以上,而
和H2O2的粒子数密度均随氧含量的增大而减小,但在考虑的氧气体积分数范围内,在水溶液中粒子渗透的初始阶段,H2O2的粒子数密度在1015cm-3以上,而 的在1013 cm-3以上,因此O3+H2O2→OH+HO2+O2主导了O3的消减。由此,随着O3的生成量增加,它的消减量同样增加,且由于
的在1013 cm-3以上,因此O3+H2O2→OH+HO2+O2主导了O3的消减。由此,随着O3的生成量增加,它的消减量同样增加,且由于 和H2O2均为长寿命粒子,所以可以在O3向深层渗透过程中一直对其产生消减作用。
和H2O2均为长寿命粒子,所以可以在O3向深层渗透过程中一直对其产生消减作用。
图8给出了O3的总生成量、总消减量及净生成量随氧气体积分数的变化。可以看到,O3的净生成量随氧含量增加而增加,因而O3的粒子数密度随氧含量增加而增加,如图3d所示。由于O3的生成主要发生在粒子刚进入液相区的阶段,但如之前指出,O3的消减在其随后的渗透过程中一直发生,因此,图3d中呈现了O3的粒子数密度在进入液相区表层后迅速下降的特点。
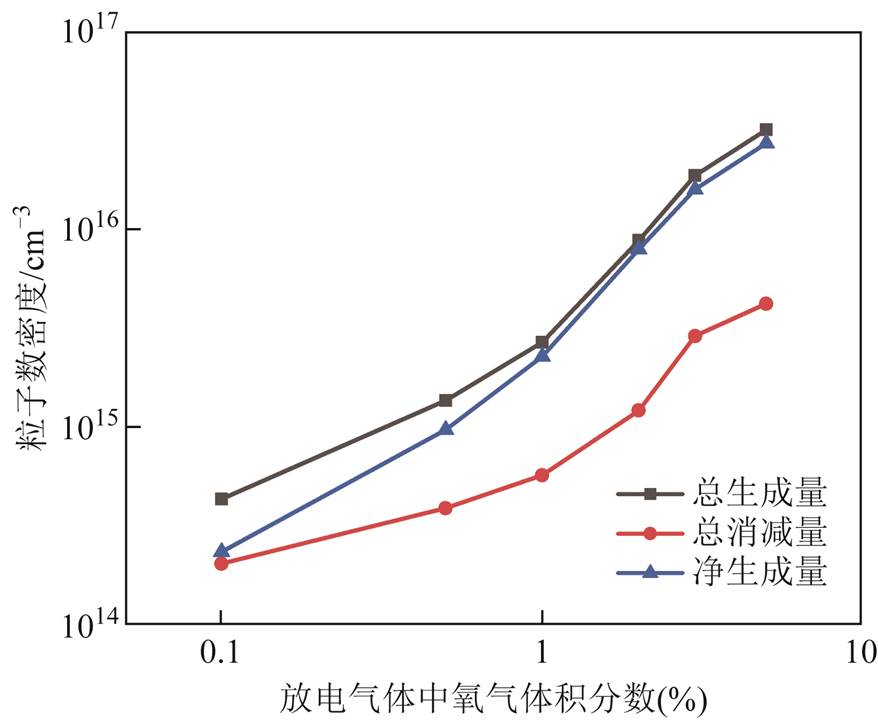
图8 不同氧气体积分数下,单位时间内O3总生成量、总消减量和总净生成量
Fig.8 Total generation quantity, total consumption quantity, and total net generation quantity of O3 in unit time as a function of oxygen volume fraction
5)OH
OH生成的主要反应有O3+H2O2→OH+HO2+O2和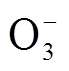 +H+→O2+OH。之前在关于O3+H2O2→OH+ HO2+ O2引起O3消减的分析中,已经表明O3消减量随氧含量增加而增加,因而由该反应生成的OH亦随氧含量增加而增加,计算得到OH生成量从3.382×1013 cm-3增大到1.568×1015 cm-3。由于
+H+→O2+OH。之前在关于O3+H2O2→OH+ HO2+ O2引起O3消减的分析中,已经表明O3消减量随氧含量增加而增加,因而由该反应生成的OH亦随氧含量增加而增加,计算得到OH生成量从3.382×1013 cm-3增大到1.568×1015 cm-3。由于 +O3→
+O3→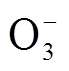 +O2随氧含量增加生成了大量的
+O2随氧含量增加生成了大量的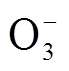 ,因此反应
,因此反应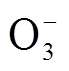 +H+→O2+OH生成的OH亦随氧含量增加而增加,从1.124×1014 cm-3上升到3.627×1015 cm-3。以上结果表明,OH的总生成量随氧含量增加而增加,且OH的两个主要生成反应均与O3有关。
+H+→O2+OH生成的OH亦随氧含量增加而增加,从1.124×1014 cm-3上升到3.627×1015 cm-3。以上结果表明,OH的总生成量随氧含量增加而增加,且OH的两个主要生成反应均与O3有关。
OH消减的主要反应包括2OH→H2O2、 OH+ →OH-+O2和OH+H2O2→HO2+H2O。后两个反应中,在考虑的氧气体积分数范围内,
→OH-+O2和OH+H2O2→HO2+H2O。后两个反应中,在考虑的氧气体积分数范围内, 和H2O2的粒子数密度比OH的大。因此,随着氧含量的增加,OH生成量增加,上述三个消减反应引起的OH消减量亦增加。
和H2O2的粒子数密度比OH的大。因此,随着氧含量的增加,OH生成量增加,上述三个消减反应引起的OH消减量亦增加。
图9为OH的总生成量、总消减量和净生成量随氧气体积分数的变化。OH净生成量随氧含量增加而增加,导致了图3e表明的OH的粒子数密度随氧含量的增加而增加。同时在图9中可以观察到,OH的生成量在相同的氧气体积分数下均远大于消减量,所以其净生成量接近于生成量,而其生成反应又均与O3有关,因此如图3e所示,OH粒子数密度的变化与O3类似,在进入液相区表层后随渗透深度增加迅速下降。
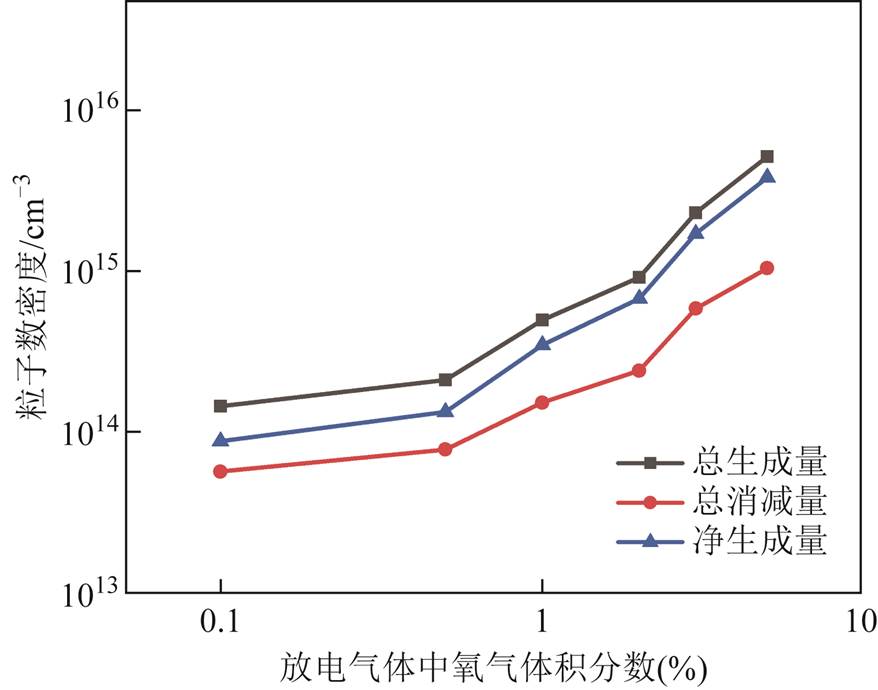
图9 不同氧气体积分数下,单位时间内OH总生成量、总消减量和总净生成量
Fig.9 Total generation quantity, total consumption quantity, and total net generation quantity of OH in unit time as a function of oxygen volume fraction
基于一维流体模型,本文对大气压He/O2等离子体在水溶液中的传质进行了数值模拟,研究了当氧气体积分数在0.1%~5%范围内,氧含量对传质中H2O2、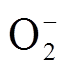 、HO2、O3及OH五种主要粒子分布的影响,得到以下结论:
、HO2、O3及OH五种主要粒子分布的影响,得到以下结论:
1)放电气体的氧含量改变影响相关氧粒子和电子进入液面的通量,进而影响五种主要活性氧粒子H2O2、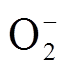 、HO2、O3和OH在水溶液中的粒子数密度和渗透深度。
、HO2、O3和OH在水溶液中的粒子数密度和渗透深度。
2)OH和O3的渗透深度随氧含量的增大而增大,在考虑的氧含量范围内,从几μm可增加到20 μm以上,这一深度使得这两种粒子可能直接作用于某些被处理物,因而对于等离子体的生物医学应用具有重要意义。
3)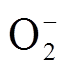 、HO2及H2O2在水溶液中的粒子数密度随氧含量的增加而减小,从而使得它们的渗透深度亦减小,但仍保持在数百微米的可观量值以上。因此,三种粒子渗透深度的减小对于它们在生物医学上的应用影响不大。
、HO2及H2O2在水溶液中的粒子数密度随氧含量的增加而减小,从而使得它们的渗透深度亦减小,但仍保持在数百微米的可观量值以上。因此,三种粒子渗透深度的减小对于它们在生物医学上的应用影响不大。
综上所述,通过增加放电气体的氧含量,既能显著地增大OH和O3的渗透深度,同时也能保持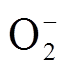 、HO2和H2O2的渗透深度在可观的量值上,从而在等离子体生物医学应用中能够更有效地利用这些重要活性氧离子的生物学作用。
、HO2和H2O2的渗透深度在可观的量值上,从而在等离子体生物医学应用中能够更有效地利用这些重要活性氧离子的生物学作用。
参考文献
[1] Kong M G, Kroesen G, Morfill G, et al. Plasma medicine: an introductory review[J]. New Journal of Physics, 2009, 11(11): 115012.
[2] Weltmann K D, von Woedtke T. Plasma medicine—current state of research and medical application[J]. Plasma Physics and Controlled Fusion, 2017, 59(1): 014031.
[3] Lu Xinpei, Reuter S, Laroussi M, et al. Nonequilibrium atmospheric pressure plasma jets: funda-mentals, diagnostics, and medical applications[M]. Boca Raton: CRC Press, 2019.
[4] 徐晗, 陈泽煜, 刘定新. 大气压冷等离子体处理水溶液:液相活性粒子检测方法综述[J]. 电工技术学报, 2020, 35(17): 3561-3582. Xu Han, Chen Zeyu, Liu Dingxin. Aqueous solutions treated by cold atmospheric plasmas: a review of the detection methods of aqueous reactive species[J]. Transactions of China Electrotechnical Society, 2020, 35(17): 3561-3582.
[5] 王瑞雪, 李忠文, 虎攀, 等. 低温等离子体化学毒剂洗消技术研究进展[J]. 电工技术学报, 2021, 36(13): 2767-2781. Wang Ruixue, Li Zhongwen, Hu Pan, et al. Review of research progress of plasma chemical warfare agents degradation[J]. Transactions of China Electrotechnical Society, 2021, 36(13): 2767-2781.
[6] 卢新培, 吴帆, 谭笑. 大气压非平衡等离子体诊断:激光散射[J]. 高电压技术, 2021, 47(10): 3684-3695. Lu Xinpei, Wu Fan, Tan Xiao. Non-equilibrium atmospheric pressure plasma diagnostic: laser scattering[J]. High Voltage Engineering, 2021, 47(10): 3684-3695.
[7] 戴栋, 宁文军, 邵涛. 大气压低温等离子体的研究现状与发展趋势[J]. 电工技术学报, 2017, 32(20): 1-9. Dai Dong, Ning Wenjun, Shao Tao. A review on the state of art and future trends of atmospheric pressure low temperature plasmas[J]. Transactions of China Electrotechnical Society, 2017, 32(20): 1-9.
[8] 张若兵, 徐莹, 张驰, 等. 双脉冲放电等离子体水处理H2O2的生成规律[J]. 高电压技术, 2010, 36(9): 2297-2302. Zhang Ruobing, Xu Ying, Zhang Chi, et al. Formation of hydrogen peroxide by bipolar pulsed discharge plasma in water[J]. High Voltage Engineering, 2010, 36(9): 2297-2302.
[9] Sardella E, Veronico V, Gristina R, et al. Plasma treated water solutions in cancer treatments: the contrasting role of RNS[J]. Antioxidants, 2021, 10(4): 605.
[10] Xu Han, Liu Dingxin, Xia Wenjie, et al. Comparison between the water activation effects by pulsed and sinusoidal helium plasma jets[J]. Physics of Plasmas, 2018, 25(1): 013520.
[11] 吴淑群, 董熙, 裴学凯, 等. 基于激光诱导荧光法诊断大气压低温等离子体射流中OH自由基和O原子的时空分布[J]. 电工技术学报, 2017, 32(8): 82-94. Wu Shuqun, Dong Xi, Pei Xuekai, et al. Laser induced fluorescence diagnostics of the temporal and spatial distribution of OH radicals and O atom in a low temperature plasma jet at atmospheric pressure[J]. Transactions of China Electrotechnical Society, 2017, 32(8): 82-94.
[12] Guo Li, Zhao Yiming, Liu Dingxin, et al. Cold atmospheric-pressure plasma induces DNA-protein crosslinks through protein oxidation[J]. Free Radical Research, 2018, 52(7): 783-798.
[13] Ikawa S, Tani A, Nakashima Y, et al. Physicochemical properties of bactericidal plasma-treated water[J]. Journal of Physics D: Applied Physics, 2016, 49(42): 425401.
[14] 李和平, 于达仁, 孙文廷, 等. 大气压放电等离子体研究进展综述[J]. 高电压技术, 2016, 42(12): 3697-3727. Li Heping, Yu Daren, Sun Wenting, et al. State-of-the-art of atmospheric discharge plasmas[J]. High Voltage Engineering, 2016, 42(12): 3697-3727.
[15] 孔刚玉, 刘定新. 气体等离子体与水溶液的相互作用研究: 意义、挑战与新进展[J]. 高电压技术, 2014, 40(10): 2956-2965. Kong M G, Liu Dingxin. Researches on the interaction between gas plasmas and aqueous solutions: significance, challenges and new progresses[J]. High Voltage Engineering, 2014, 40(10): 2956-2965.
[16] 夏文杰, 刘定新. Ar等离子体射流处理乙醇水溶液的放电特性及灭菌效应[J]. 电工技术学报, 2021, 36(4): 765-776. Xia Wenjie, Liu Dingxin. Discharge characteristics and bactericidal effect of Ar plasma jet treating ethanol aqueous solution[J]. Transactions of China Electrotechnical Society, 2021, 36(4): 765-776.
[17] Sun Yi, Yu Shuang, Sun Peng, et al. Inactivation of Candida biofilms by non-thermal plasma and its enhancement for fungistatic effect of antifungal drugs[J]. PLoS One, 2012, 7(7): e40629.
[18] Traylor M J, Pavlovich M J, Karim S, et al. Long-term antibacterial efficacy of air plasma-activated water[J]. Journal of Physics D: Applied Physics, 2011, 44(47): 472001.
[19] Jiang Jixiang, Tan Zhenyu, Shan Chunhong, et al. A new study on the penetration of reactive species in their mass transfer processes in water by increasing the electron energy in plasmas[J]. Physics of Plasmas, 2016, 23(10): 103503.
[20] Pan Jie, Tan Zhenyu, Liu Yadi, et al. Effects of oxygen concentration on atmospheric-pressure pulsed dielectric barrier discharges in argon/oxygen mixture[J]. Physics of Plasmas, 2015, 22(9): 093515.
[21] Wang Xiaolong, Tan Zhenyu, Han Jiaqi, et al. Numerical investigation on electron effects in the mass transfer of the plasma species in aqueous solution[J]. Plasma Science and Technology, 2020, 22(11): 115504.
[22] Liu D W, Iza F, Kong M G. Electron heating in radio-frequency capacitively coupled atmospheric- pressure plasmas[J]. Applied Physics Letters, 2008, 93(26): 261503.
[23] Zhang Yuantao, Lou Jie, Li Qingquan, et al. Electrode-gap effects on the electron density and electron temperature in atmospheric radio-frequency discharges[J]. IEEE Transactions on Plasma Science, 2013, 41(3): 414-420.
[24] Zhao Bo, Mattelaer F, Rampelberg G, et al. Thermal and plasma-enhanced atomic layer deposition of yttrium oxide films and the properties of water wettability[J]. ACS Applied Materials & Interfaces, 2020, 12(2): 3179-3187.
[25] Kojtan A, Ercan U K, Smith J, et al. Chemistry for antimicrobial properties of water treated with non-equilibrium plasma[J]. Journal of Nanomedicine & Biotherapeutic Discovery, 2013, 4(1): 1000120.
[26] Chen C, Liu D X, Liu Z C, et al. A model of plasma-biofilm and plasma-tissue interactions at ambient pressure[J]. Plasma Chemistry and Plasma Processing, 2014, 34(3): 403-441.
[27] Bergmann M E H. Drinking water disinfection by In-line electrolysis: product and inorganic by-product formation[M]// Comninellis C, Chen Guohua. Electrochemistry for the Environment. New York: Springer, 2009: 163-204.
[28] Cutler R G, Rodriguez H. Critical reviews of oxidative stress and aging: advances in basic science, diagnostics and intervention[M]. Hackensack: World Scientific Publishing Company, Incorporated, 2002.
[29] Pierini P, Appel P, Newman J. Current distribution on a disk electrode for redox reactions[J]. Journal of the Electrochemical Society, 1976, 123(3): 366-369.
[30] Liu Z C, Liu D X, Chen C, et al. Physicochemical processes in the indirect interaction between surface air plasma and deionized water[J]. Journal of Physics D: Applied Physics, 2015, 48(49): 495201.
[31] Venkatadri R, Peters R W. Chemical oxidation technologies: ultraviolet light/hydrogen peroxide, Fenton’s reagent, and titanium dioxide-assisted photocatalysis[J]. Hazardous Waste and Hazardous Materials, 1993, 10(2): 107-149.
[32] Rumbach P, Bartels D M, Sankaran R M, et al. The effect of air on solvated electron chemistry at a plasma/liquid interface[J]. Journal of Physics D: Applied Physics, 2015, 48(42): 424001.
Abstract Cold-temperature atmospheric plasma (CAP) has been successfully applied in biological engineering, such as sterilization, surgery and even cancer treatment. However, the biological tissue to be treated is usually covered with a layer of aqueous solution with a thickness of tens to hundreds of microns. Plasma action on the surface of biological tissues necessarily involves the mass transfer process of the active species generated by the plasma in aqueous solution. There are lots of experimental measurement techniques have been used to analyze the mass transfer process between plasma and water. However, due to the limited detection technology, it is difficult to obtain the concentration distribution of species in aqueous solution. Thus, we used numerical simulations to quantify the mass transfer of active species in aqueous solutions.
Based on the one-dimensional diffusion-reaction model, the mass transfer process of active species produced in plasma from the gas phase region to the gas-liquid interface region and finally into the liquid phase region is investigated in this work by establishing the control equations and boundary conditions of liquid phase region. The generation of active species in the plasma is closely related to the oxygen volume in the discharge gas,so we analyzed the generation and consumption reactions of active species in aqueous solution by simulating 19 reactive oxygen species (ROS) and 84 main chemical reactions in the liquid phase region with the change of the oxygen volume fraction in the discharge gas (the range is 0.1%~5%), in order to study the penetration depth distribution of the five main ROSs (H2O2, 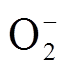 , HO2, O3, and OH) in liquid phase region under different conditions. According to the simulation, the change of oxygen volume in the discharge gas has an impact on the flux of active species generated by the plasma into the liquid phase region, which also affects the generation and consumption of the five main ROS in the aqueous solution.For H2O2,
, HO2, O3, and OH) in liquid phase region under different conditions. According to the simulation, the change of oxygen volume in the discharge gas has an impact on the flux of active species generated by the plasma into the liquid phase region, which also affects the generation and consumption of the five main ROS in the aqueous solution.For H2O2, 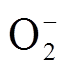 , and HO2, all the generation, consumption, and net generation decrease with the increase of oxygen content, while for the OH and O3, all the generation, consumption, and net generation increase with increase of oxygen content. These processes finally results in the change of the species number density and penetration depth of the ROS.
, and HO2, all the generation, consumption, and net generation decrease with the increase of oxygen content, while for the OH and O3, all the generation, consumption, and net generation increase with increase of oxygen content. These processes finally results in the change of the species number density and penetration depth of the ROS.
The following conclusions can be drawn from the simulation analysis: (1)The change of the oxygen content volume in the discharge gas affects the flux of related oxygen species and electrons into the liquid surface, and then affects the species number density concentration and penetration of the five ROSs in the aqueous solution depth. (2)The penetration depth of OH and O3 increases with the increase of oxygen volume, from a few μm to more than 20 μm within the range of oxygen volume considered, this depth makes it possible for these two species to act directly on some biological tissue. (3)The species number density of H2O2, 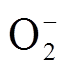 , and HO2 in aqueous solution decreases with the increase of oxygen volume, so their penetration depth also decreases, but they still remains above a considerable value of hundreds of microns. Therefore, the reduction of the penetration depth of the three particles has little effect on their biomedical applications.
, and HO2 in aqueous solution decreases with the increase of oxygen volume, so their penetration depth also decreases, but they still remains above a considerable value of hundreds of microns. Therefore, the reduction of the penetration depth of the three particles has little effect on their biomedical applications.
keywords:Plasma species mass transfer, helium/oxygen mixture, oxygen concentration effect, one-dimensional fluid model, plasma biomedicine
DOI: 10.19595/j.cnki.1000-6753.tces.220212
中图分类号:TM8
国家自然科学基金(52077128)和山东省自然科学基金(ZR2020ME208)资助项目。
收稿日期 2022-02-14
改稿日期 2022-05-10
丁蕴函 男,1999年生,硕士研究生,研究方向为气体放电等离子体。E-mail:qingdaodyh@126.com
王晓龙 男,1979年生,副教授,硕士生导师,研究方向为气体放电等离子体。E-mail:wangxiaolong@sdu.edu.cn(通信作者)
(编辑 李冰)