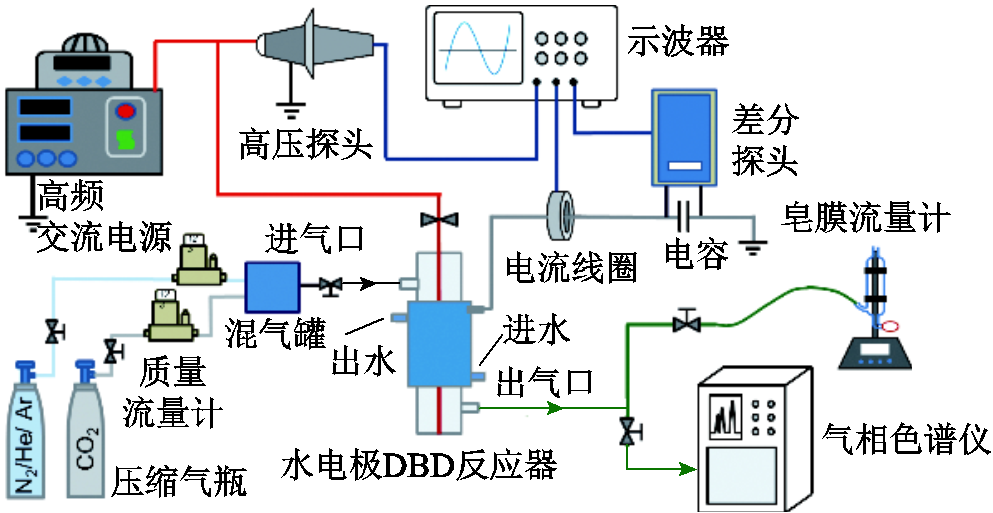
图1 实验装置及测量系统
Fig.1 The experimental device and measurement system
摘要 大气压低温等离子体能够打破热力学平衡的限制,促使常规情况下难以发生的反应在温和条件下进行。其中,介质阻挡放电(DBD)在CO2转化利用领域受到了广泛的关注,但是其性能受多种因素影响。该文采用水电极同轴介质阻挡放电反应装置进行CO2直接分解反应,研究分析添加N2、Ar和He及其不同含量对反应过程放电特性及反应效果的影响。结果表明:相同反应条件下,在CO2气氛中添加N2、Ar和He可以增加微放电通道数量,提高放电功率,降低击穿电压,使更多的能量用于活化反应体系分子,但三种气体对放电过程的影响程度明显不同;对比添加气体N2、Ar和He,在CO2转化效果上表现为Ar>He>N2,这主要是由于添加Ar后反应体系具有最高的电子碰撞激发反应速率,在Ar含量为80%时,CO2的转化率最大为15.2%,CO的产率最大为9.3%;但是,上述气体的添加会降低CO2的能量转化效率,其中,N2添加下转化CO2的能量效率下降最为明显,由0.08mmol/kJ下降到0.02mmol/kJ。该文研究成果可以为低温等离子体转化CO2过程的优化提供有益参考。
关键词:水电极介质阻挡放电 CO2直接分解 气体添加 放电特性 能量效率
近年来,化石燃料能源的大规模开采利用和人类活动向大气中排放了大量的CO2,导致温室效应不断累积,全球气候不断变暖,从而引发了一系列的环境问题,直接威胁到人类与动植物的健康[1]。CO2排放问题不仅涉及能源环境问题,更是上升到了关乎人类社会可持续发展的高度,解决CO2排放问题刻不容缓。
CO2资源化利用是将CO2变废为宝,转化为具有高附加值的化工产品,既能满足社会日益增长的能源需求,又能从根本上实现CO2减排,符合绿色可持续发展的理念[2]。现有用于CO2资源化利用的常规方法主要有热解法、光催化转化法、电催化转化法、光电还原法等。但是,由于CO2分子具有很强的热力学和动力学稳定性,上述方法在运行条件、能量利用率、转化率和选择性、催化剂制备与活性保持、经济成本、环境保护等方面存在局限性[3]。
近年来,大气压低温等离子体技术的迅速发展为CO2高效资源化利用提供了新的思路和方法[4-8]。介质阻挡放电(Dielectric Barrier Discharge, DBD)作为一种产生大气压低温等离子体的主要形式,具有反应器结构简单、设计灵活、操作方便、放电稳定均匀、能够激发活化通过反应器的全部气体等特点,易于从实验室用装置升级为工业应用设备,已经在废气处理和臭氧合成等实际应用领域积累了丰富的成功经验[9-14],因而,受到了等离子体CO2转化领域的广泛关注,具有良好的应用前景。
针对DBD等离子体转化CO2,国内外研究人员从反应过程放电特性、转化效果和效率、反应机理和机制等角度开展了大量的研究工作,考察了DBD反应器结构、激励电源类型及参数、运行条件参数、反应物成分及比例、添加填充材料或催化剂等因素对DBD转化CO2过程,尤其是CO2转化率和能量效率的影响[15-18]。近年来,研究人员发现将水电极DBD用于CO2转化反应可表现出良好的性能。Zhou Amin等发现水电极DBD中CO2直接分解转化率是普通DBD反应器的两倍以上[19]。Wang Li等研究发现采用水电极DBD可以有效促进CO2转化过程液态产物甲醇的生成[20]。为改善DBD放电特性并提高CO2转化反应性能,研究人员在反应体系中添加He、Ar和N2等气体,在提高CO2转化率方面取得了一定的效果,但是气体添加将消耗部分放电等离子体能量,进而降低过程能量效率,如何选择添加气体及其添加比例需要进一步研究。目前,关于水电极DBD反应器中添加气体对CO2转化过程放电特性及CO2转化性能的研究相对偏少,缺乏指导用于CO2转化的水电极DBD反应器优化和过程性能提升的数据。鉴于此,本文采用水电极DBD进行CO2直接分解反应,并向反应体系中添加不同浓度的N2、He和Ar,以考察添加气体及其浓度对CO2直接分解过程电气特性和反应性能的影响,研究结果将为优化DBD反应器及CO2转化系统设计、提升CO2转化反应性能提供有益参考。
实验装置及测量系统示意如图1所示,包括反应器、激励电源、供气系统、放电特性诊断和反应产物分析设备等。采用交流电源作为驱动电源,电压幅值和频率范围分别为0~30kV和0~20kHz,实验过程中输入电压和频率分别固定在18kV和10kHz。采用自行设计的水电极同轴DBD反应器,阻挡介质为石英玻璃管,其内、外径分别为8mm和10mm;内电极为光滑的不锈钢棒,不锈钢棒直径为4mm,长度为35cm,与驱动电源的高压端相连接;循环水作为外电极,经外接电容后接地,循环水温度由冰水混合物来控制,近似保持在0℃。采用红外热像仪(Fotric 223s)对放电间隙温度进行测量,发现本文工况范围内放电间隙气体温度在155~170℃之间变化。在进行纯CO2直接分解的基础上,添加N2、Ar和He三种气体,各气体由压缩气瓶提供,采用质量流量计(北京七星,MFC,D07—19)控制和调节气体流量,分别调节上述气体的含量在0~80%范围内变化,控制气体总流量为50mL/min。

图1 实验装置及测量系统
Fig.1 The experimental device and measurement system
采用高压探头(Tek P6015A,分压比为1 000∶1)和电流线圈(Pearson Electronics Inc,6585)分别测量反应器输入电压和总电流;采用差分探头(Pintech,N1070A,分压比为1 000∶1)测量外接电容两端的电压,用于计算放电回路中传输电荷等参数;采用四通道数字示波器(Tektronix,TDS2014B)记录保存上述电压电流信号;采用数字式皂膜流量计测量反应后气体总流量;采用气相色谱仪(天美,GC7900)测量反应后气体产物中各组分含量。
1.2.1 电气特性分析方法
电气特性主要通过分析电压电流波形和Lissajous图形获得。纯CO2直接分解时的电压电流波形如图2所示。图中,电压U(t)波形表现为近似光滑的正弦曲线,电流I(t)波形表现为凸起的丝状曲线,以多脉冲形式出现,对应于DBD放电过程微放电通道,电流脉冲的大小和数量可以用来分析放电强度。基于电流波形,可采用Origin软件工具箱计量不同工况下电流脉冲个数来分析电流特性,具体过程见参考文献[21]。
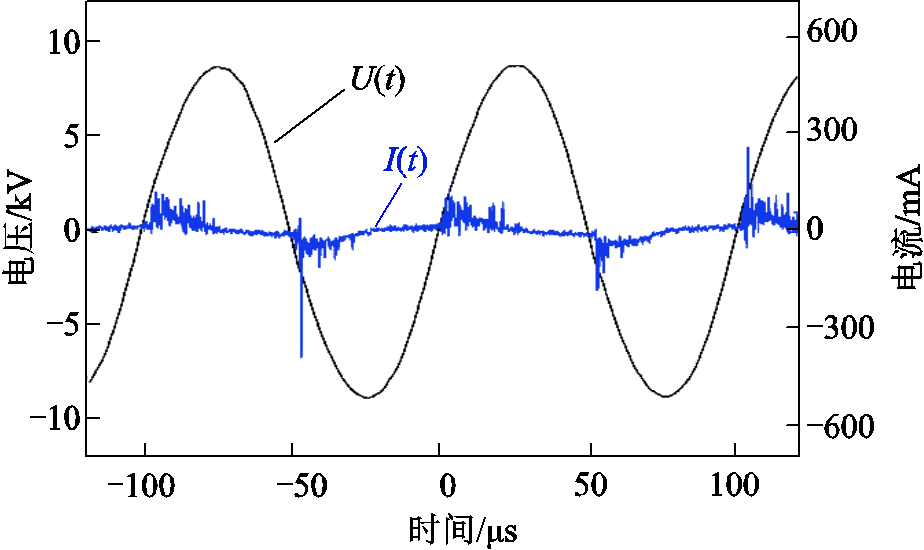
图2 纯CO2分解时电压电流波形
Fig.2 The voltage-current waveforms in the process of pure CO2 decomposition
典型的DBD Lissajous图形如图3所示,一般近似为平行四边形[22-23]。
图3中,边DA和CB表示未放电的时间段,这两条边的斜率为未形成放电时DBD反应器的总电容Ccell,此电容值还可表示为
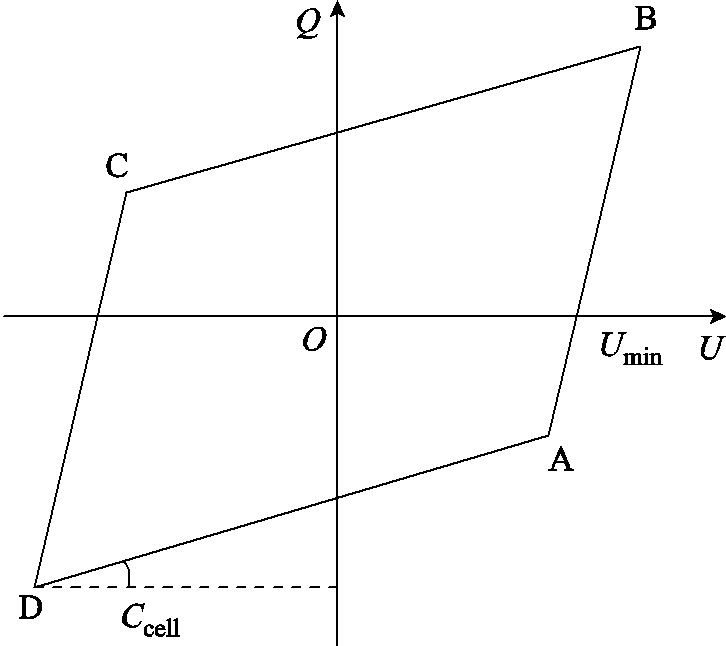
图3 典型的DBD Lissajous图形
Fig.3 Typical Lissajous figure for DBD
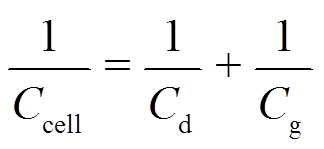 (1)
(1)
式中,Cd和Cg分别为DBD反应器介质层和气体间隙的电容值[23-24]。这两个电容值理论上可以通过式(2)和式(3)计算得到[22-23],即
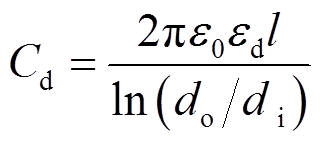 (2)
(2)
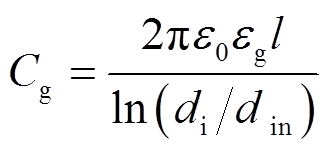 (3)
(3)
式中,din、di、do和l分别为内电极直径、介质管内径、外径及放电长度,其中l由水电极的长度决定,其值为6cm;ε0、εd和εg分别为真空介电常数、石英介质和反应气体的相对介电常数,ε0=8.854×10-12F/m,εd=3.70[22]。由于本文研究中反应气体为混合气体,其相对介电常数εg未知,因而采用式(3)不能获得气体电容。本文由根据Lissajous图形得到的Ccell值和由式(2)计算得到的Cd值,通过式(1)计算获得Cg。在此基础上,由式(4)进一步计算获得击穿电压UB,该值表示起始放电时气隙的电压值[24],即
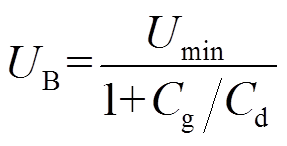 (4)
(4)
式中,Umin为放电起始的最小外加电压,可从图3的Lissajous图形中获得。基于Lissajous图形,通过式(5)可计算放电功率P为
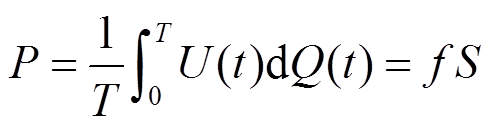 (5)
(5)
式中,T、f、S分别为输入电压的周期、频率及Lissajous图形的面积;Q(t)为t时刻的电荷量。
1.2.2 CO2分解效果评价
CO2直接分解反应性能的评价指标主要有CO2转化率(X)、CO产率(Y)和能量效率(Energy Efficiency, EE),分别为
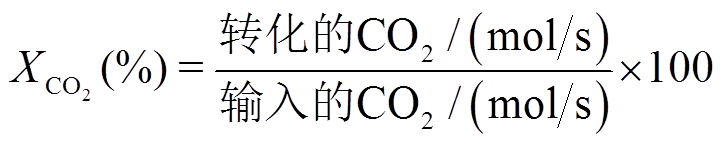 (6)
(6)
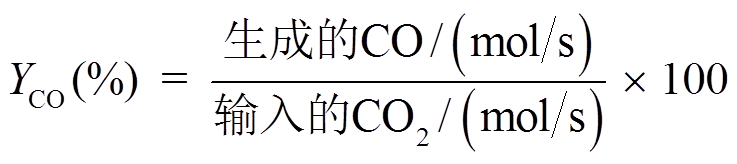 (7)
(7)
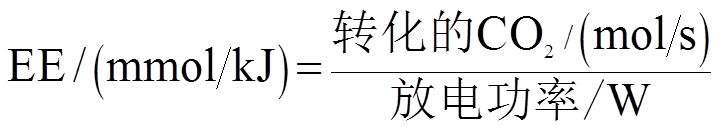 (8)
(8)
不同气体的添加明显改变了CO2气体DBD的放电特性。N2、He、Ar的添加比例为60%时的电压电流波形如图4所示。可以看出,在外加电压的正负半周期均产生放电,电流波形呈现为大量微放电的脉冲形式,电流脉冲不均匀分布在每个电压周期内。在输入电压的正负半周期内,电流脉冲出现较为明显的不对称性,这主要是由于不对称电极造成的[25-26]。对比图2所示的纯CO2分解过程的电压电流波形,上述气体的添加显著提高了电流脉冲的幅值、数量和持续时间,且不同的气体表现出不同的影响。添加N2后电流脉冲的波动最大,出现少量峰值接近600mA的电流脉冲;添加He后电流脉冲的波动最为平缓,电流脉冲峰值在300mA以内;而添加Ar后电流脉冲的波动介于两者之间。添加He和Ar后的电流脉冲的持续时间明显高于添加N2的情况,例如,添加N2后正负半周期内电流脉冲的持续时间约为20μs和14μs,而添加He和Ar后持续时间则分别约为24μs和13μs、26μs和15μs。总体而言,添加不同气体后电流脉冲幅值平均值由大到小的变化顺序为Ar>N2>He。根据上述情况,结合已有研究发现,添加Ar后CO2直接分解体系具有最高的电子密度[23,27],具体可参见本文后续结果分析与讨论部分的半定量计算和分析。
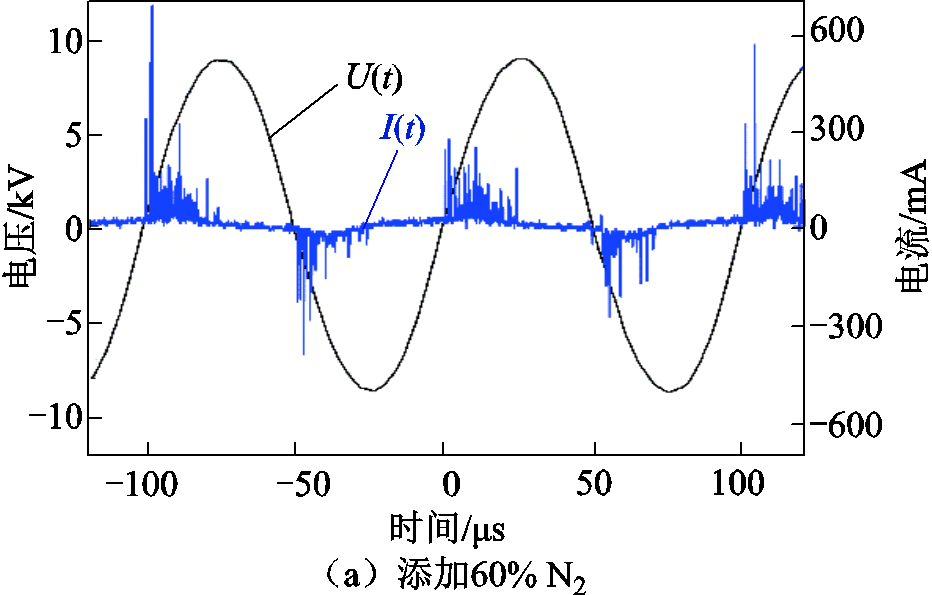
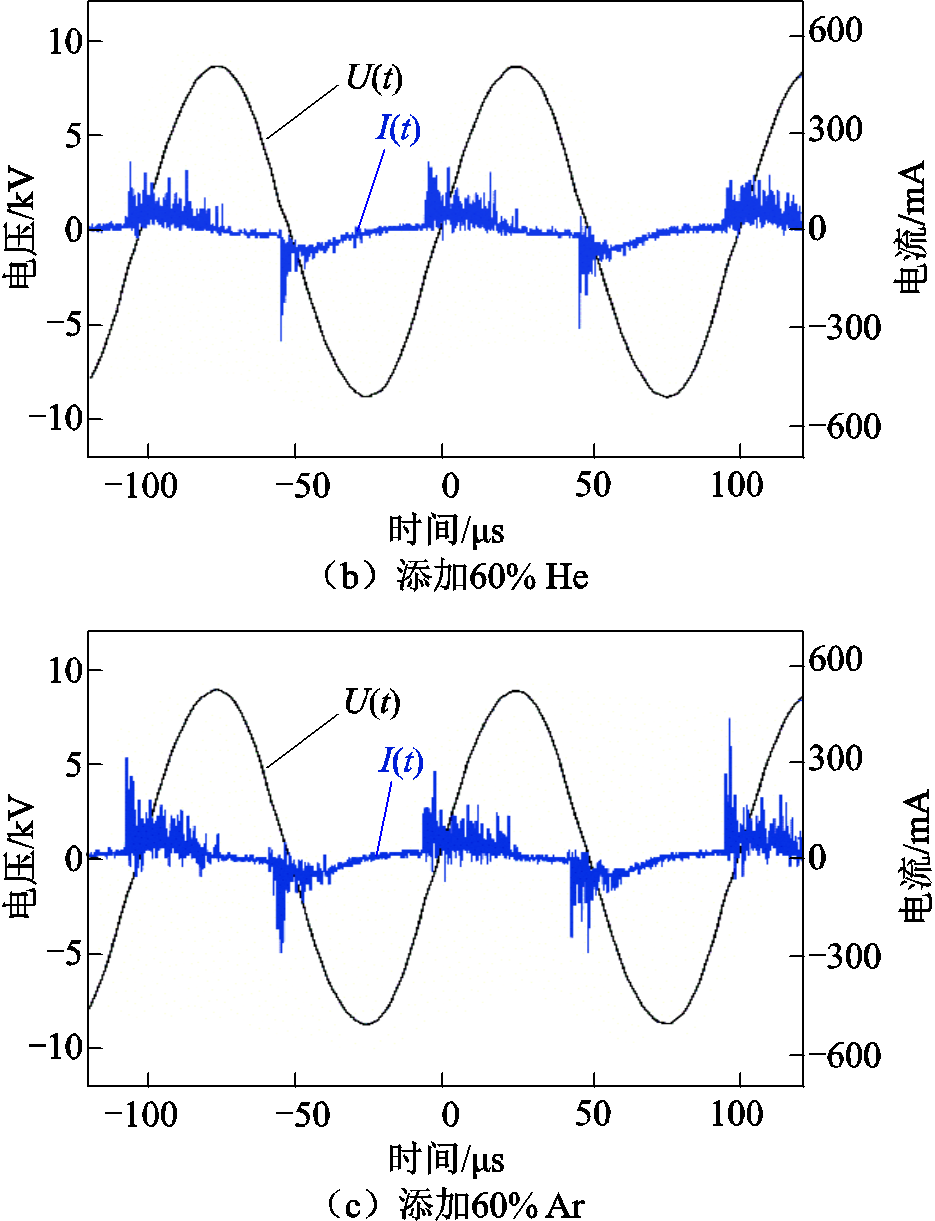
图4 气体成分对CO2分解过程电压电流波形的影响
Fig.4 Effect of gas composition on the voltage-current waveforms in CO2 decomposition
为深入理解不同气体成分对CO2分解过程电流特性的影响,不同气体成分及其添加比例情况下CO2分解过程中每个周期内的电流脉冲数量如图5所示。很明显,添加N2、He和Ar可显著增加电流脉冲数目。其中,添加N2后电流脉冲数目增幅最低,且受添加比例的影响最小,添加20%的N2时,电流脉冲数量提高42.0%,而N2添加比例提升至80%,电流脉冲数量增幅仅为14.1%;添加Ar后电流脉冲数目增幅最高,且受添加比例的影响也最大,仅添加20%的Ar,电流脉冲数目的增幅高达98.0%,进一步提升Ar添加比例至80%,电流脉冲数目增幅仍为44.4%;添加不同比例He对电流脉冲数目的影响介于两者之间。上述电流脉冲数的变化表明,不同比例N2、He和Ar的添加将增加气体间隙内的微放电通道,以利于CO2直接分解反应的进行。

图5 不同添加气体及比例对CO2分解过程每个周期内电流脉冲数量的影响
Fig.5 Effect of gas addition and its concentration on the number of current pulses per cycle in CO2 decomposition
图6所示为添加不同比例的N2、He和Ar所对应的Lissajous图形。从图中可以看出,当纯CO2直接分解时,Lissajous图形表现为边长近似相等的平行四边形,N2的添加及其添加比例变化对Lissajous图形几乎没有影响;添加低浓度的He和Ar对Lissajous图形的影响也不大,但是随着这两种气体添加比例的提升,Lissajous图形发生明显的变化,由原来边长近似相等的平行四边形逐渐变化为扁平的平行四边形,且添加比例越大,Lissajous图形越扁。可以看出,添加不同比例的N2、He和Ar将直接影响CO2分解过程的放电功率和击穿特性。
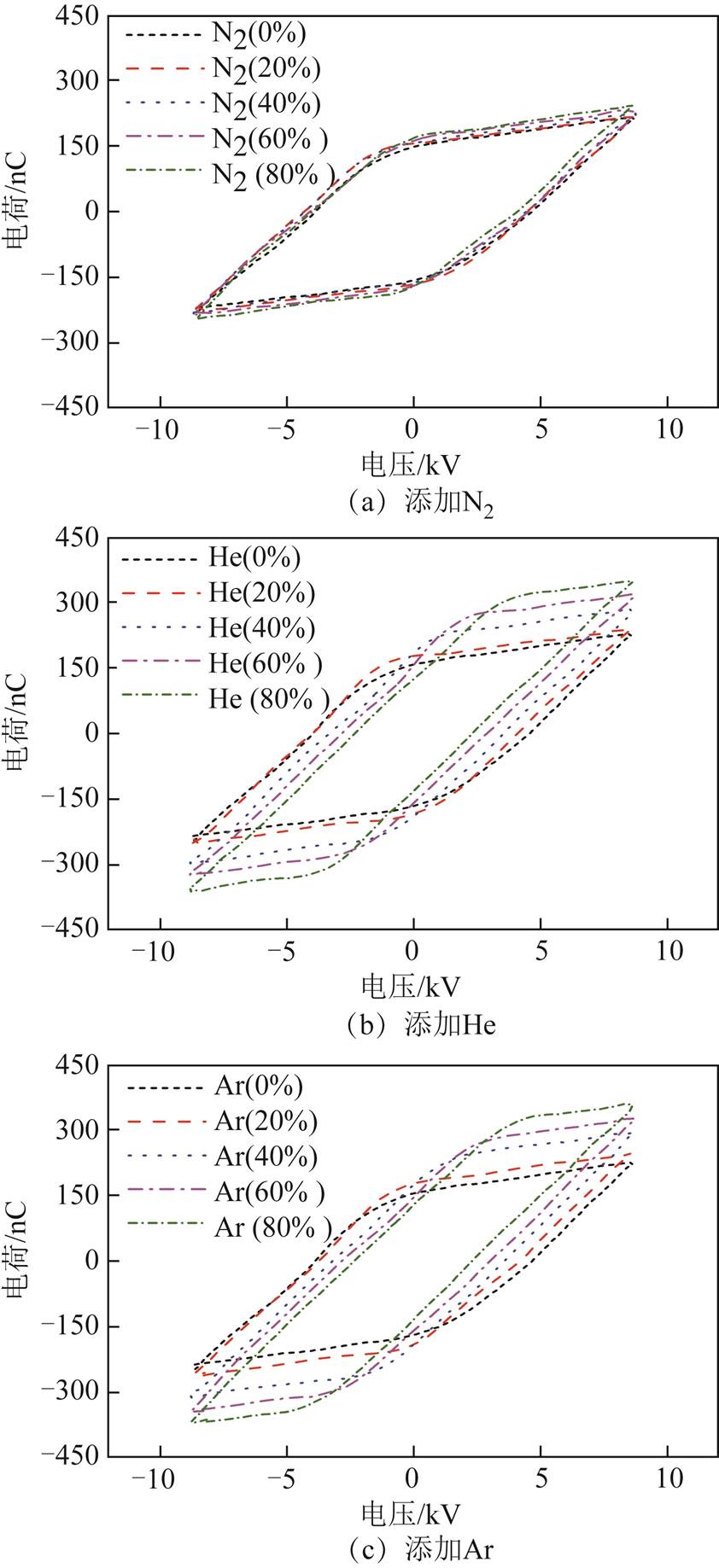
图6 不同添加气体对CO2分解过程Lissajous图形的影响
Fig.6 Effect of gas addition on the Lissajous figures of CO2 decomposition
利用Lissajous计算得到的添加不同气体时的放电功率P和击穿电压UB如图7所示。从图中可以看出,随着N2、He和Ar添加比例的增加,放电功率逐渐增加,但增加速率较为平缓,不同工况下放电功率均在31~38W之间变化;且添加不同气体时放电功率的区别不明显,在相同条件下,添加He和Ar时的放电功率略高于添加N2时的情况。添加这三种气体均降低了CO2分解过程的击穿电压,且不同气体及其添加比例对于击穿电压的影响表现出了明显的区别,例如从未添加气体到添加80%的N2,击穿电压下降幅度最低,仅为9.7%,而添加He和Ar则明显降低了放电击穿电压,并以添加He时作用最为明显,当He添加比例从0%变化为80%时,击穿电压下降幅度达50%。上述现象的产生主要从两方面来考虑:①已有研究表明在特定的约化电场强度(E/N,E为电场强度,N为粒子数密度)和压力条件下,纯Ar、He和N2的汤森电离系数α要高于纯CO2的情况,这说明与纯CO2相比,CO2/Ar、CO2/He和CO2/N2气氛中单位长度能产生更多的电子,从而降低击穿电压[23,28];②Ar、He、N2分子电子碰撞激发和电离的电子能量阈值分别为11.5eV和15.8eV、19.8eV和24.6eV、7.7eV和14.5eV,高于CO2分子对应的电子能量阈值6.2eV和13.8eV,这将降低混合气氛中非弹性碰撞的概率,使更多的能量用于电子碰撞激发和解离CO2分子[23,28-29]。从图7可以看出,随着气体添加比例的提高,放电功率表现出相似的缓慢增加趋势,而击穿电压降低,尤其是当添加He和Ar时降低幅度非常明显,这表明添加这三种气体后更多的能量用于激发活化反应体系分子,而非击穿气体,这是添加气体提高CO2转化率的主要原因之一。M. Ramakers和M. A. Lindon等的研究也得到了相似的结论[23,30]。

图7 不同添加气体对CO2分解过程放电功率与击穿电压的影响
Fig.7 Effect of gas addition on discharge power and breakdown voltage of CO2 decomposition process
不同气体添加工况对等离子体直接分解CO2过程中CO2转化率的影响如图8所示。从图中可以看出,在进行纯CO2直接分解时,CO2的转化率为6.7%,当N2、He和Ar的添加比例为20%时,CO2转化率分别为7.0%、7.2%和7.5%;随着添加气体比例的增加,CO2转化率继续上升,在添加气体含量为80%时,CO2转化率分别提高到7.3%、13.2%和15.2%;添加N2时CO2转化率增幅最小,仅为9.2%,添加Ar时的增幅最大,为125.6%,而添加He时的增幅介于两者之间,为96.0%。添加不同气体成分对CO2直接分解主要产物CO产率的影响如图9所示,图中也表现出了类似的规律,当添加气体比例从0%上升至80%时,添加N2、He和Ar的体系中CO产率的增幅分别为25.5%、57.4%和97.9%。
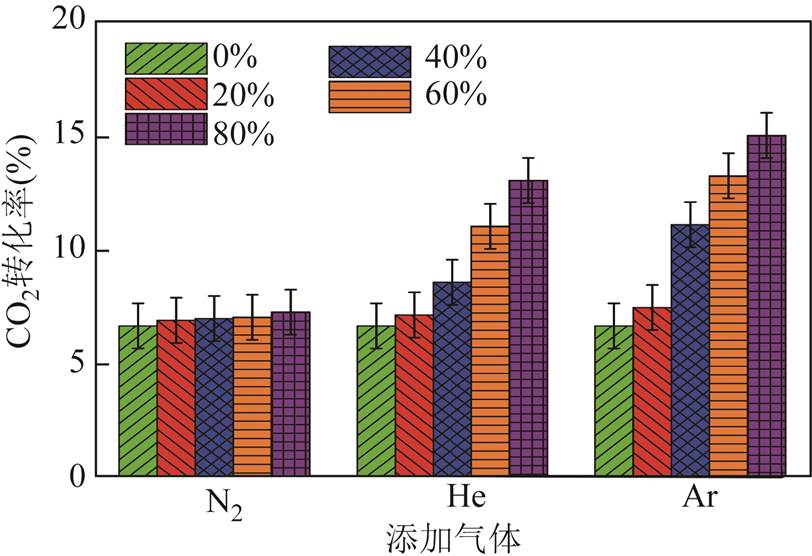
图8 不同添加气体对CO2转化率的影响
Fig.8 Effect of gas addition on CO2 conversion
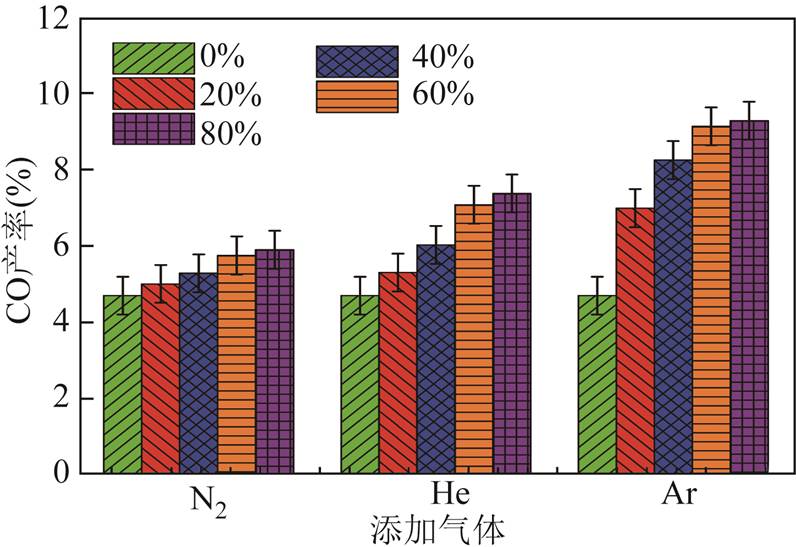
图9 不同添加气体对CO产率的影响
Fig.9 Effect of gas addition on the yield of CO
不同气体添加工况对等离子体直接分解CO2过程中能量效率的影响如图10所示。从图中可以看出,随着气体添加比例的增加,水电极同轴DBD转化CO2的能量效率相应减少。其中,CO2/N2混合条件下转化CO2的能量效率下降较为明显,由0.08mmol/kJ下降到0.02mmol/kJ;CO2/He和CO2/Ar混合条件下转化CO2的能量效率均由0.08mmol/kJ下降到0.03mmol/kJ。由电气特性分析可知,在本文研究工况条件下,各工况放电功率差别不明显,而随着气体添加比例的增加,一部分能量被用于激发活化N2、He或Ar以产生激发态、电离态等成分,虽然上述活性成分将促使CO2活化转化,但未能弥补直接用于CO2分解能量的减少[23],最终降低了被转化的CO2的绝对数量,导致能量效率的降低。在后续研究中将进一步优化反应器结构和运行参数,并筛选出适用于水电极DBD环境进行CO2分解转化的高性能催化剂,以期提高反应能量效率。
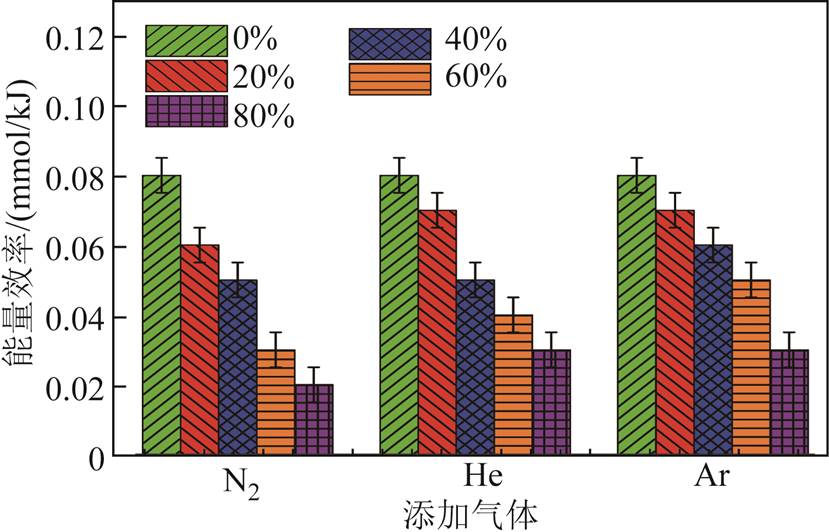
图10 不同添加气体对能量效率的影响
Fig.10 Effect of gas addition on energy efficiency
前期研究表明振动激发转化是低温等离子体中最节能高效的CO2转化反应路径,在电子能量为1~2eV的等离子体环境中,电子振动激发占整个CO2分解反应路径的比例高达97%[31]。而DBD反应体系中电子平均能量较高(>2eV),R. Aerts等通过零维等离子体化学反应动力学仿真发现,在DBD条件下CO2分解转化是由电子碰撞激发基态CO2分子来实现的[32],即
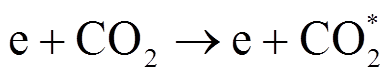 (9)
(9)
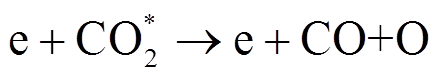 (10)
(10)
式中,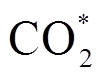 为激发态CO2分子。本文后续将通过半定量计算来分析不同工况下电子密度、平均电子能量及电子碰撞激发反应速率,以理解添加不同气体及其不同比例对CO2分解转化过程的影响。
为激发态CO2分子。本文后续将通过半定量计算来分析不同工况下电子密度、平均电子能量及电子碰撞激发反应速率,以理解添加不同气体及其不同比例对CO2分解转化过程的影响。
在典型的DBD约化电场强度E/N=200Td(Td为约化电场强度单位,1Td=1×10-17V·cm2)条件下[33],采用开源软件BOLSIG+[34]计算添加不同气体时CO2分解体系的平均电子能量和电子碰撞激发反应速率常数,并结合实验测得的电流波形,通过式(11)估算不同条件下的电子密度[23],得到
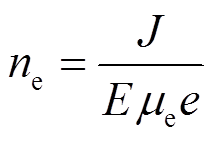 (11)
(11)
式中,J、E、μe和e分别为电流密度、电场强度、电子迁移率和单位电荷。其中,电流密度由实验获得的半个周期内电流幅值平均值除以单个微放电截面积估算获得,后者采用文献值1.05×10-6m2[35]。实际放电过程中多个微放电细丝同时存在且相互作用,因此该方法只能半定量地粗略估算电子密度[23],但这也足以分析不同添加气体对CO2分解反应性能的影响。电场强度由E/N=200Td计算获得;电子迁移率由BOLSIG+计算得到;单位电荷值为1.6×10-19C。
不同气体添加工况对反应体系平均电子能量和和电子碰撞激发反应速率常数的影响如图11所示。从图中可以看出,不同添加气体对平均电子能量的影响趋势不同。当N2的添加比例从0%提高至80%时,平均电子能量下降了11.5%。Xu Shaojun等发现在填充床DBD分解CO2体系中添加N2后平均电子能量也有所下降[28]。而添加He和Ar则提高了体系平均电子能量,且添加He后平均电子能量提升最为明显,为26.1%,这符合M. Ramakers等的研究结果趋势[23]。可以发现,电子碰撞激发反应速率常数和平均电子能量随不同气体添加的变化趋势是一致的,这主要是由于电子碰撞激发反应速率常数和电子能量直接相关[23]。
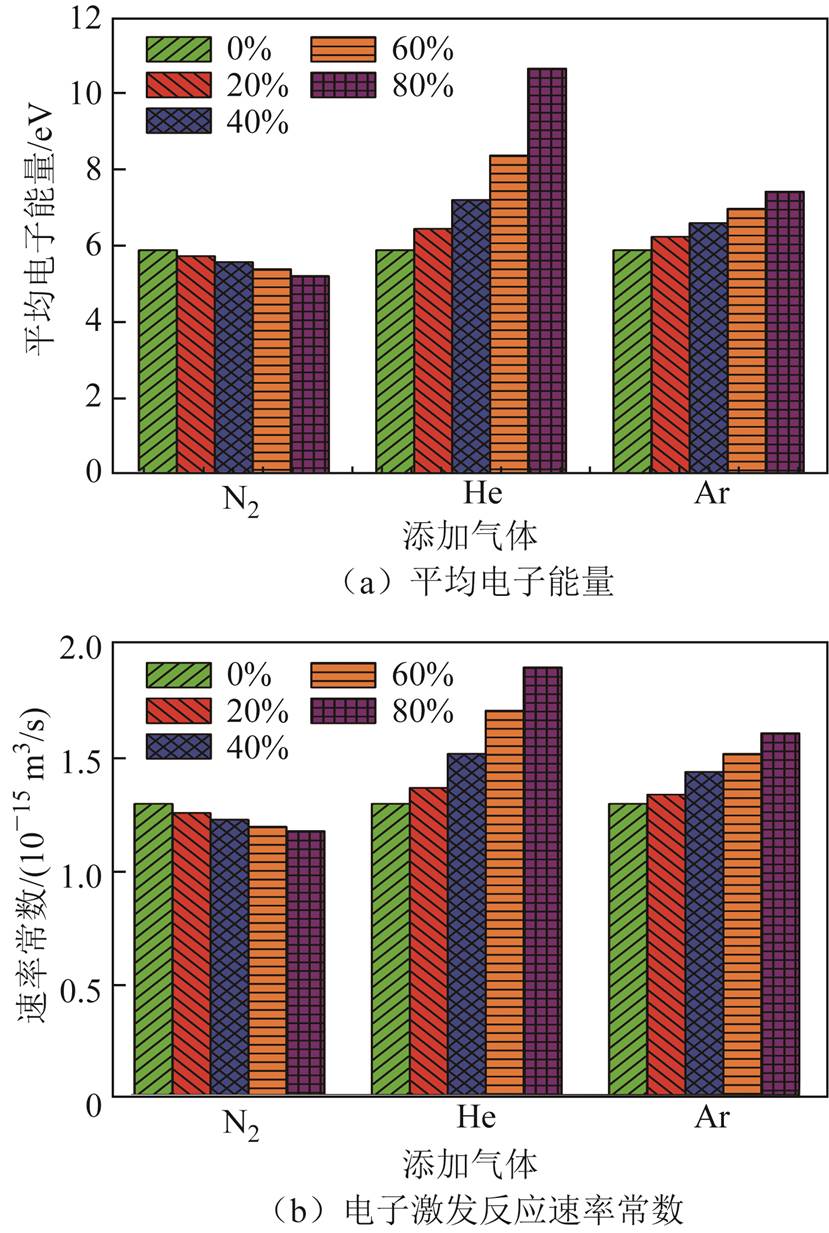
图11 不同添加气体对平均电子能量和电子激发反应速率常数的影响
Fig.11 Effect of gas addition on mean electron energy and rate constant for electron impact excitation
不同气体添加工况对反应体系平均电子密度和电子碰撞激发反应速率的影响如图12所示。可以看出,当反应体系中添加N2和Ar时,提高添加气体浓度将增加电子密度,且添加Ar时增幅最大,当其添加比例从0%提高至80%时,电子密度增加54.8%。而随着He添加比例的提高,电子密度出现缓慢下降的趋势,这一结果和M. Ramakers等的研究结果有所区别,在他们的研究中,He的添加比例为95%,此时,放电电流波形中电流脉冲的幅值很小,放电更接近均匀的模式,放电电流密度小,导致和纯CO2的反应体系相比,电子密度明显降低[23]。而本文的研究中He添加比例的变化范围为0%~80%,虽然电流平均值随着添加比例的提高略有降低,但仍然具有明显的电流脉冲,且持续时间较长,表现为典型的丝状放电。将电子密度与反应速率常数相乘即可获得电子碰撞激发反应的速率[23],如图12b所示,从图中可以看出电子碰撞激发反应速率随添加气体及其添加比例的变化趋势与CO2转化率的变化规律是一致的,即添加Ar时电子碰撞激发反应速率增幅最大,添加He时次之,而添加N2时增幅最小,这是三种添加气体及其比例对CO2转化过程反应物转化率产生不同影响的主要原因。
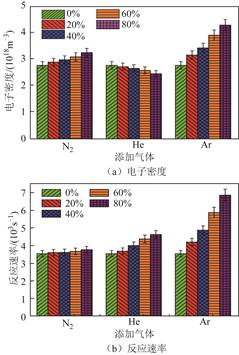
图12 不同添加气体对电子密度和电子碰撞激发反应速率的影响
Fig.12 Effect of gas addition on electron density and reaction rate for electron impact excitation
除上述主要原因之外,不同反应体系中形成的主要活性成分对反应过程也会产生重要影响。例如添加N2时,电子激发产生的亚稳态氮分子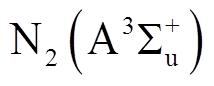 将使CO2发生碰撞解离,即
将使CO2发生碰撞解离,即
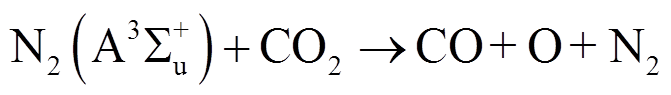 (12)
(12)
该反应的贡献度随着N2含量的增加而明显提升[29],且它可以作为反应气体参与到化学反应中,本身解离后可以与体系中CO反应生成NCO,促使化学平衡向右移动,更有利于促进CO2的分解,这在其他文献中也有报道[18,29]。当添加Ar时,体系中电离态成分(如Ar+)和CO2发生电荷交换反应,可直接解离CO2分子,或者先产生电离态CO2+,后者在电子碰撞反应下进一步解离为CO和O[23],即
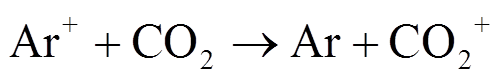 (13)
(13)
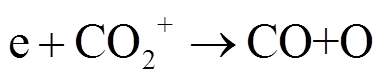 (14)
(14)
在添加He的反应体系中,同样存在电荷交换反应,但是和Ar相比,He的电离能(24.6eV)高于前者(15.8eV),在相同的电压和气体成分条件下,反应体系中生成的电离态He成分(He+或者He2+)要少于添加Ar的情况[23],因而,对于CO2分解转化反应的贡献度要低于Ar。综合上述分析,添加这三种气体对CO2分解转化的贡献度由大到小为Ar>He>N2。
本文考察了不同气体添加对水电极同轴DBD中CO2直接分解过程的电气特性及反应效果的影响,对气体添加后的电信号进行了测量和分析,并测试了不同气体添加情况下CO2的分解反应效果。主要结论如下:
1)在水电极DBD直接分解CO2体系中添加N2、He和Ar将提高反应体系微放电通道数量,且随着气体添加比例的增加,提升效果更加明显。此外,添加这三种气体在缓慢增加放电功率的同时,降低了击穿电压,使更多的能量用于分解CO2,而非击穿气体。
2)添加Ar和He将增加平均电子能量和电子碰撞激发反应速率常数,且添加He时增幅更加明显,但添加N2会降低上述两个参数;反应体系电子密度则随着添加N2和Ar比例的增加而提高,添加He使电子密度缓慢降低;结合反应速率常数和电子密度,发现电子碰撞激发反应速率均随着添加比例的提高而增加,且增幅趋势为Ar>He>N2。此外,反应体系中的N2、He、Ar的激发态、电离态等活性成分,增加了CO2分解转化的反应途径,进一步提高CO2转化率和CO产率。三种气体添加对转化效果提升表现为不同的特点:当N2、He和Ar添加比例从0%增加至80%,CO2转化率增幅分别为9.2%、96.0%和125.6%。
3)由于反应体系中气体添加将消耗部分放电等离子体能量,生成可促进CO2分解转化的活性成分,但并不能弥补直接用于CO2分解能量的减少,降低了反应过程的能量效率。本文研究中发现,在未添加气体时获得最大能量效率,为0.08mmol/kJ。优化反应器结构和运行参数、选用合适的高性能催化剂是后续提高反应过程能量效率的可行措施。
参考文献
[1] Clark M A, Domingo N G G, Colgan K, et al. Global food system emissions could preclude achieving the 1.5°and 2℃climate change targets[J]. Science, 2020, 370(6517): 705-708.
[2] Hepburn C, Adlen E, Beddington J, et al. The technological and economic prospects for CO2 utilization and removal[J]. Nature, 2019, 575(7781): 87-97.
[3] Modak A, Bhanja P, Dutta S, et al. Catalytic reduction of CO2 into fuels and fine chemicals[J]. Green Chemistry, 2020, 22(13): 4002-4033.
[4] 王晓玲, 高远, 张帅, 等. 脉冲参数对介质阻挡放电等离子体CH4干重整特性影响的实验[J]. 电工技术学报, 2019, 34(6): 1329-1337.
Wang Xiaoling, Gao Yuan, Zhang Shuai, et al. Effects of pulse parameters on dry reforming of CH4 by pulsed DBD plasma[J]. Transactions of China Electrote-chnical Society, 2019, 34(6): 1329-1337.
[5] 戴栋, 宁文军, 邵涛. 大气压低温等离子体的研究现状与发展趋势[J]. 电工技术学报, 2017, 32(20): 1-9.
Dai Dong, Ning Wenjun, Shao Tao. A review on the state of art and future trends of atmospheric pressure low temperature plasmas[J]. Transactions of China Electrotechnical Society, 2017, 32(20): 1-9.
[6] Huang Bangdou, Zhang Cheng, Bai Han, et al. Energy pooling mechanism for catalyst-free methane activation in nanosecond pulsed non-thermal plasmas[J]. Chemical Engineering Journal, 2020, 396: 125185.
[7] Wang Weizong, Berthelot A, Kolev S, et al. CO2 conversion in a gliding arc plasma: 1D cylindrical discharge model[J]. Plasma Sources Science and Technology, 2016, 25(6): 065012.
[8] 陈赦, 刘红梅, 吴婷, 等. 低温等离子体增强催化氨合成机理的一维流体动力学模型[J]. 电工技术学报, 2021, 36(13): 2730-2739.
Chen She, Liu Hongmei, Wu Ting, et al. 1D fluid model of catalytic ammonia synthesis enhanced by low temperature plasma[J]. Transactions of China Electrotechnical Society, 2021, 36(13): 2730-2739.
[9] 鲁娜, 张楚珂, 夏芸, 等. 等离子体转化CO2的研究进展[J]. 高电压技术, 2020, 46(1): 351-361.
Lu Na, Zhang Chuke, Xia Yun, et al. Advances in plasma technology for CO2 conversion research[J]. High Voltage Engineering, 2020, 46(1): 351-361.
[10] 梅丹华, 方志, 邵涛. 大气压低温等离子体特性与应用研究现状[J]. 中国电机工程学报, 2020, 40(4): 1339-1358, 1425.
Mei Danhua, Fang Zhi, Shao Tao. Recent progress on characteristics and applications of atmospheric pressure low temperature plasmas[J]. Proceedings of the CSEE, 2020, 40(4): 1339-1358, 1425.
[11] 杨勇, 梅丹华, 段戈辉, 等. 不同电源激励Ar同轴介质阻挡放电特性对比[J]. 高电压技术, 2020, 46(12): 4355-4364.
Yang Yong, Mei Danhua, Duan Gehui, et al. Comparison of discharge characteristics of Ar coaxial dielectric barrier discharge dirven by different power supplies[J]. High Voltage Engineering, 2020, 46(12): 4355-4364.
[12] Kogelschatz U. Dielectric-barrier discharges: their history, discharge physics, and industrial applications[J]. Plasma Chemistry and Plasma Processing, 2003, 23(1): 1-46.
[13] 张晓星, 王宇非, 崔兆仑, 等. 不同填充材料对介质阻挡放电降解SF6的实验研究[J]. 电工技术学报, 2021, 36(2): 397-406.
Zhang Xiaoxing, Wang Yufei, Cui Zhaolun, et al. Experimental study on the degradation of SF6 by dielectric barrier discharge with different packing materials[J]. Transactions of China Electrotechnical Society, 2021, 36(2): 397-406.
[14] 张龙龙, 崔行磊, 刘峰, 等. 不同类型电源激励下HMDSO添加比例对Ar介质阻挡放电特性的影响[J]. 电工技术学报, 2021, 36(15): 3135-3146.
Zhang Longlong, Cui Xinglei, Liu Feng, et al. Effect of HMDSO addition ratio on Ar DBD characteristics excited by different types of power sources[J]. Transactions of China Electrotechnical Society, 2021, 36(15): 3135-3146.
[15] Wang Li, Du Xiaomin, Yi Yanhui, et al. Plasma-enhanced direct conversion of CO2 to CO over oxygen-deficient Mo-doped CeO2[J]. Chemical Communications, 2020, 56(94): 14801-14804.
[16] Li Ju, Zhai Xingwu, Ma Cunhua, et al. DBD plasma combined with different foam metal electrodes for CO2 decomposition: experimental results and DFT validations[J]. Nanomaterials, 2019, 9(11): 1595.
[17] Yap D, Tatibouët J M, Batiot-Dupeyrat C. Carbon dioxide dissociation to carbon monoxide by non-thermal plasma[J]. Journal of CO2 Utilization, 2015, 12: 54-61.
[18] Xu Shaojun, Khalaf P I, Martin P A, et al. CO2 dissociation in a packed-bed plasma reactor: effects of operating conditions[J]. Plasma Sources Science and Technology, 2018, 27(7): 075009.
[19] Zhou Amin, Chen Dong, Dai Bin, et al. Direct decomposition of CO2 using self-cooling dielectric barrier discharge plasma[J]. Greenhouse Gases: Science and Technology, 2017, 7(4): 721-730.
[20] Wang Li, Yi Yanhui, Guo Hongchen, et al. Atmospheric pressure and room temperature synthesis of methanol through plasma-catalytic hydrogenation of CO2[J]. ACS Catalysis, 2018, 8(1): 90-100.
[21] Ozkan A, Dufour T, Silva T, et al. The influence of power and frequency on the filamentary behavior of a flowing DBD—application to the splitting of CO2[J]. Plasma Sources Science and Technology, 2016, 25(2): 025013.
[22] Mei Danhua, Zhu Xinbo, He Yaling, et al. Plasma-assisted conversion of CO2 in a dielectric barrier discharge reactor: understanding the effect of packing materials[J]. Plasma Sources Science and Technology, 2014, 24(1): 015011.
[23] Ramakers M, Michielsen I, Aerts R, et al. Effect of argon or helium on the CO2 Conversion in a dielectric barrier discharge[J]. Plasma Processes and Polymers, 2015, 12(8): 755-763.
[24] Tu Xin, Gallon H J, Twigg M V, et al. Dry reforming of methane over a Ni/Al2O3 catalyst in a coaxial dielectric barrier discharge reactor[J]. Journal of Physics D: Applied Physics, 2011, 44(27): 274007.
[25] Duan Gehui, Fang Zhi, Fu Junhui, et al. Influence of water cooling for outer electrode on the discharge characteristics of an atmospheric coaxial DBD reactor[J]. IEEE Transactions on Plasma Science, 2021, 49(3): 1173-1180.
[26] Belov I, Paulussen S, Bogaerts A. Appearance of a conductive carbonaceous coating in a CO2 dielectric barrier discharge and its influence on the electrical properties and the conversion efficiency[J]. Plasma Sources Science and Technology, 2016, 25(1): 015023.
[27] Aerts R, Somers W, Bogaerts A. Carbon dioxide splitting in a dielectric barrier discharge plasma: a combined experimental and computational study[J]. ChemSusChem, 2015, 8(4): 702-716.
[28] Xu Shaojun, Whitehead J C, Martin P A. CO2 conversion in a non-thermal, barium titanate packed bed plasma reactor: the effect of dilution by Ar and N2[J]. Chemical Engineering Journal, 2017, 327: 764-773.
[29] Snoeckx R, Heijkers S, van Wesenbeeck K, et al. CO2 conversion in a dielectric barrier discharge plasma: N2 in the mix as a helping hand or problematic impurity?[J]. Energy & Environmental Science, 2016, 9(3): 999-1011.
[30] Lindon M A, Scime E E. CO2 dissociation using the Versatile atmospheric dielectric barrier discharge experiment (VADER)[J]. Frontiers in Physics, 2014, 2: 55.
[31] Fridman A. Plasma chemistry[M]. Cambridge: Cambridge University Press, 2008.
[32] Aerts R, Martens T, Bogaerts A. Influence of vibrational states on CO2 splitting by dielectric barrier discharges[J]. The Journal of Physical Chemistry C, 2012, 116(44): 23257-23273.
[33] Bogaerts A, Kozák T, van Laer K, et al. Plasma-based conversion of CO2: current status and future challenges[J]. Faraday Discussions, 2015, 183: 217-232.
[34] Hagelaar G J M, Pitchford L C. Solving the Boltzmann equation to obtain electron transport coefficients and rate coefficients for fluid models[J]. Plasma Sources Science and Technology, 2005, 14(4): 722-733.
[35] Valdivia-Barrientos R, Pacheco-Sotelo J, Pacheco-Pacheco M, et al. Analysis and electrical modelling of a cylindrical DBD configuration at different operating frequencies[J]. Plasma Sources Science and Technology, 2006, 15(2): 237-245.
Abstract CO2 conversion and utilization can convert the greenhouse gas into valuable fuels and chemicals, rather than regarding it as a waste. Due to the high stability of CO2 molecules, the traditional methods for CO2 conversion have limitations in terms of operating conditions, conversion and selectivity, catalyst preparation and activity maintenance. The rapid development of atmospheric pressure non-thermal plasma technology has provided new approaches for CO2conversion. Dielectric barrier discharge (DBD), as a main form of non-thermal plasma, has received extensive attention in the field of plasma CO2 conversion. The performance of this process is affected by various factors, and it has been found that using the DBD reactor with water electrode and adding auxiliary gas (e.g., He, Ar and N2) can improve the reaction performance to a certain extent. However, the research on the discharge characteristics and the reaction performance of CO2 conversion in a DBD reactor with water electrode and auxiliary gas addition is limited. It is still unclear how to optimize the reaction process and performance. To address these issues, the direct decomposition of CO2 has been performed in a DBD reactor with water electrode. The auxiliary gases He, Ar and N2 are added into reactant stream with different concentrations to evaluate their influence on electrical characteristics and reaction performance of direct CO2 decomposition process.
The DBD reactor is self-designed using quartz tube and stainless-steel rod. A casing tube is formed with two quartz tubes and the water at 0℃ circulates inside the casing tube, acting as the low voltage electrode. The stainless-steel rod is set coaxially with the inner quartz tube and acts as the high voltage electrode. The low voltage electrode is grounded after connecting to a reference capacitor. The DBD reactor is powered by custom-built AC power source. A Tektronix high-voltage probe and a Pearson current coil monitor are used to collect the applied voltage and the total current, while a Pintech differential probe is used to sample the voltage across the reference capacitor. All of these signals have been saved using a Tektronix digital oscilloscope. A Techcomp gas chromatography (GC) is used to analyze the gaseous products. The electrical characteristics has been obtained by analyzing the voltage-current wave forms and the Lissajous figure. Based on the voltage-current wave forms, the number of current spikes and the electron density are determined. While the discharge power and the breakdown voltage are calculated according to the Lissajous figure. The open-source software BOLSIG+ has been used to determine the average electron energy and the rate constant for electron impact excitation. The reaction rate for electron impact excitation is obtained by the electron density and the rate constant. The reaction performance is evaluated by the parameters of CO2 conversion, CO yield and energy efficiency.
The following conclusions can be drawn: ① adding He, Ar and N2 increases the discharge channels, and this effect is enhanced by increasing the concentrations of these gases. In addition, adding these gases increases the discharge power while reducing the breakdown voltage, so that more energy is used for the excitation of the gas molecules. ② Adding Ar and He increases the average electron energy and rate constant for electron impact excitation, but adding N2 reduces these two parameters. Meanwhile, adding N2 and Ar increases the electron density, which was reduced by adding He. Combing the electron density and the rate constant, the reaction rate for electron impact excitation is increased by increasing the concentration of these auxiliary gases, and the increasing trend follows the order of Ar>He>N2. ③For the reaction performance, the effect of these auxiliary gases also follows the order of Ar>He>N2. The highest CO2 conversion and CO yield is 15.2% and 9.3%, respectively, in the presence of 80% Ar. However, adding these gases reduces the process energy efficiency. Optimizing the reactor structure and operating parameters, and exploring a suitable high-performance catalyst are the feasible approaches to improve the process energy efficiency.
keywords:Dielectric barrier discharge with water electrode, direct decomposition of CO2, gas addition, electrical characteristics, energy efficiency
DOI:10.19595/j.cnki.1000-6753.tces.211442
中图分类号:TM85
陈慧敏 女,1996年生,硕士研究生,研究方向为大气压低温等离子体特性诊断及能源转化应用。E-mail:CHM2021@njtech.edu.cn
梅丹华 男,1985年生,副教授,硕士生导师,研究方向为高电压与气体放电等离子体技术及其能源环境应用。E-mail:danhuam@126.com(通信作者)
国家自然科学基金(51807087,52177149)、江苏省自然科学基金(BK20180705)、江苏省“六大人才高峰”创新人才团队项目(TD-JNHB-006)和电力设备电气绝缘国家重点实验室开放课题(EIPE19208)资助项目。
收稿日期 2021-09-09
改稿日期 2021-12-20
(编辑 李冰)