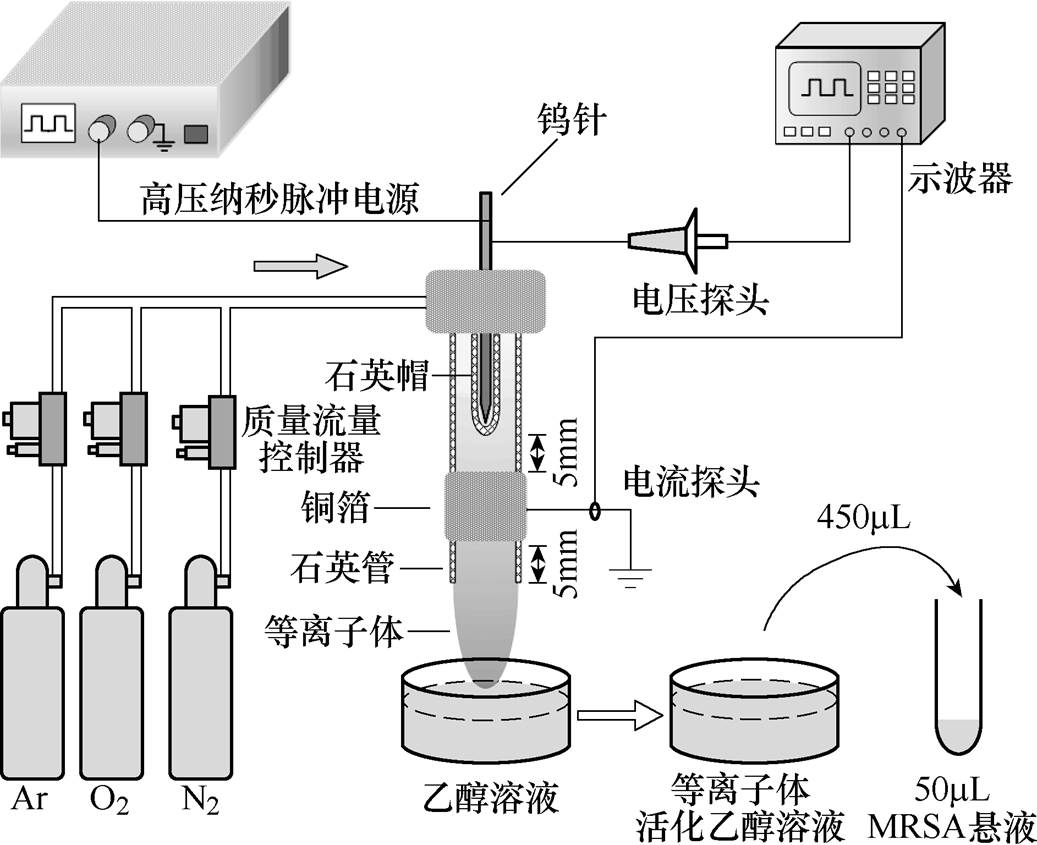
图1 Ar等离子体射流处理乙醇溶液及PAES灭菌装置
Fig.1 The device of ethanol solution treated by Ar plasma jet and PAES used for sterilization
摘要 乙醇是一种医疗上常用的消毒剂,理论上在Ar等离子体射流处理的水溶液中掺杂乙醇可以增强灭菌效果。通过对耐甲氧西林金黄色葡萄球菌的灭活实验,发现在被处理的水溶液中掺杂20%乙醇可使Ar射流等离子体活化水的灭菌效果提高5个数量级以上。进一步地,发现当工作气体中掺杂0.2%N2或在屏蔽罩中掺杂1%O2时,只需在被处理的水溶液中掺杂2%乙醇,即可提高5个数量级以上的灭菌效果。同时发现,2%乙醇掺杂可使等离子体中多个放电通道交叠,原因可能是亚稳态Ar*和乙醇气体分子在气液界面的彭宁电离作用。最后,通过对液相活性粒子的检测分析,发现等离子体活化乙醇溶液中的过氧乙酸可能在灭菌过程中起主导作用,而过氧亚硝酸和过氧乙酸可能协同作用增强了灭菌效果。
关键词:Ar等离子体射流 乙醇 放电特性 灭菌效应
近年来,大气压等离子体射流由于可以直接将等离子体中的短寿命活性粒子和带电粒子作用于生命体并诱导生物医学效应,在癌症治疗、伤口愈合、消毒与灭菌等领域的研究和应用得到了快速发 展[1-5]。在这些应用中,被处理的生物物质往往处于潮湿或液体环境中,使得等离子体与水溶液的相互作用不可避免[6-7]。同时,国内外学者发现等离子体产生的紫外辐射、局部热场、强电场、带电粒子以及活性粒子等可通过改变细胞所处液相环境(主要是液相活性粒子的改变)而产生生物医学效应[2]。一般认为,等离子体与水溶液相互作用产生的活性氧粒子(Reactive Oxygen Species, ROS)和活性氮粒子(Reactive Nitrogen Species, RNS)在生物医学效应中起着最关键作用[8-10]。这些ROS和RNS可分为长寿命活性粒子,如过氧化氢(H2O2)、臭氧(O3)、硝酸(HNO3/NO3-)、亚硝酸(HNO2/NO2-)等,以及短寿命活性粒子,如羟基(·OH)、超氧阴离子(O2·-/HOO·)、过氧亚硝酸(ONOOH/·ONOO-)、过氧硝酸(O2NOOH/O2NOO-)等[11-17]。
然而,等离子体射流由于放电功率和处理面积较小,在较短时间内与水溶液相互作用产生的液相ROS和RNS浓度往往较低。在一些对化学活性要求较高的生物医学应用中,如微生物灭活,等离子体射流很难在短时间内达到理想的处理效果,尤其是对水溶液中多重耐药微生物的灭活。例如:Ma Ruonan等采用Ar+2%O2等离子体射流处理去离子水10min,再用生成的等离子体活化水处理金黄色葡萄球菌15min,发现只能使其细菌菌落数(Colony- Forming Unit, CFU)降低1.9个数量级[18];Xu Yingyin等采用Ar+2%O2等离子体射流处理去离子水20min,再用等离子体活化水处理好氧嗜常温菌5min,发现只能取得0.22个数量级的灭菌效果[19];Xia Wenjie等分别采用Ar和Ar+0.08%O2等离子体射流处理耐甲氧西林金黄色葡萄球菌(Methicillin- Resistant Staphylococcus aureus, MRSA)悬液5min,发现都没有灭菌效果[20]。因此,如何提升等离子体射流与水溶液相互作用产生的液相ROS和RNS的成分和浓度,以增强生物医学应用效果,是等离子体射流在生物医学领域应用和发展的关键问题。
值得注意的是,乙醇是一种医疗上常用的消毒剂,但是高浓度的乙醇对伤口具有强烈的刺激性,而低浓度的乙醇对耐药微生物的灭活效果较差。理论上,等离子射流与乙醇溶液相互作用可以产生协同灭菌效应。同时,相比于价格昂贵的氦气,氩气(Ar)是一种较为便宜的稀有气体[21-23]。因此,在工业大规模应用中,Ar常作为工作气体来产生等离子体[24-26]。本文针对Ar等离子体射流处理水溶液,研究了被处理的水溶液中少量乙醇掺杂对放电特性和灭菌效应的影响。首先,对比了放电和不放电两种情况下Ar射流等离子体活化乙醇溶液(Plasma- activated Ethanol Solution, PAES)和乙醇溶液对MRSA的灭活效果。为了增强PAES的灭菌效果,同时降低乙醇对伤口的刺激性,进一步研究了低乙醇浓度下工作气体中不同O2或N2掺杂浓度对灭菌效果的影响。通过放电特性和发射光谱分析,提出在屏蔽罩中通入Ar+O2以优化PAES灭菌效果的方法。最后,通过液相活性粒子检测分析,阐述PAES的灭菌机理。
图1展示了Ar等离子体射流处理乙醇溶液以及PAES用于灭菌处理的实验装置。等离子体射流源采用针-环电极结构,高压电极采用石英帽包裹的钨针电极,与高压纳秒脉冲电源相连;环形接地电极则由10mm宽的铜箔包裹在石英管外构成,位于气流下游端。高压针电极与环形接地电极、环形接地电极与石英管管口的间距都为5mm。石英管的内径为4.0mm,外径为6.0mm。工作气体通路包含Ar、O2和N2三条气体支路。通过质量流量控制器分别产生Ar、Ar+O2混合气体和Ar+N2混合气体三种工作气体,并通入等离子体射流源中,总气体流量都为5L/min。其中,O2或N2掺杂比控制为0.08%、0.2%、0.5%、1%。为了保证Ar等离子体射流能作用到乙醇溶液的液面,高压纳秒脉冲电源的电压幅值选定为8.0kV,频率选定为23kHz,脉宽选定为6.0ms。待处理的乙醇溶液(体积为1.0mL)置于直径为15mm的石英圆皿中,液面和石英管管口的间距为15mm。
在实验测量中,采用高压电压探头Tektronix P6015A和电流探头Pearson 2877分别测量电压幅值和流经地电极的电流。通过泰克示波器Tektronix MDO3054(带宽为500MHz,采样频率为2.5GS/s)对电压和电流波形进行采集。放电图像由数码相机Nikon D7000拍摄,曝光时间为1.0s。等离子体时空演化过程的图像由型号为PI-MAX3的增强型电荷耦合装置(Intensified Charge-Coupled Device, ICCD)相机拍摄,曝光时间为20ns。同时,采用型号为SR750的Andor光学发射光谱仪对石英管管口处的辐射激发态粒子进行检测,发射光谱检测范围为300~800nm,分辨率0.015nm。此外,采用型号为SQD2的Waters H-Class UPLC液相色谱-质谱联用仪和型号为EXM+的Bruker电子自旋共振波谱仪对等离子体活化乙醇溶液中的活性粒子进行检测。实验中采用捕捉剂TEMPONE-H与等离子体活化乙醇溶液中的·ONOO-/O2·-反应生成自旋加合物TEMPONE·。自旋加合物谱线通过电子自旋共振波谱仪测得,并通过SpinFit软件进行拟合排除噪声干扰,再通过双积分值与自由基浓度的线性关系换算得到样品中加合物的浓度。浓度换算的线性关系采用TEMPONE˙标准曲线的换算公式。

图1 Ar等离子体射流处理乙醇溶液及PAES灭菌装置
Fig.1 The device of ethanol solution treated by Ar plasma jet and PAES used for sterilization
在PAES灭菌实验中,采用微生物灭活实验中常用的耐甲氧西林金黄色葡萄球菌作为研究对象,实验重复3次。具体过程如下:
(1)MRSA悬液制备。首先,将MRSA在4mL的胰蛋白胨大豆肉汤(Tryptone Soybean Broth, TSB)液体培养基中37℃过夜培养。然后,将300mL培养液转移到30mL的TSB液体培养基中进一步37℃培养3h,再以4 000r/min的速度离心2min,接着在生理盐水溶液中重悬MRSA。通过紫外-可见分光光度计检测MRSA悬浮液的吸光度,也即光密度(Optical Density, OD)。其在波长lmax= 600nm处有最大吸收强度,从而制备OD600=1的MRSA悬液,其浓度约为1×109CFU·mL-1。
(2)PAES灭活MRSA。首先,在等离子体射流活化1mL乙醇溶液5min后,立即搅拌石英皿中的PAES 5s。然后,用移液枪将450mL的PAES转移到含有50mL MRSA悬液的离心管中,孵化5min。
(3)细菌存活菌落数统计。采用10倍梯度稀释法在磷酸缓冲盐溶液中对处理后的MRSA悬液(5× 107CFU·mL-1)进行稀释,然后在TSB琼脂板上进行涂布,每个稀释浓度取3个10mL的样品,培养24h后统计细菌菌落数即可计算出每毫升处理后的细菌悬浮液中存活的细菌菌落总数。
图2展示了放电和不放电两种情况下PAES和乙醇溶液对MRSA的灭活效果。结果表明,不放电时40%以上的乙醇溶液可以取得5个数量级以上显著的灭菌效果(***p<0.001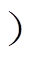 ;但低于20%的乙醇溶液对MRSA的灭活效果可以忽略不计,相较于对照组无明显统计学差异。而放电时PAES的灭菌效果随着乙醇浓度的增加逐渐增强;当乙醇浓度为5%时,PAES的灭菌效果相较于对照组显著增加(***p<0.001
;但低于20%的乙醇溶液对MRSA的灭活效果可以忽略不计,相较于对照组无明显统计学差异。而放电时PAES的灭菌效果随着乙醇浓度的增加逐渐增强;当乙醇浓度为5%时,PAES的灭菌效果相较于对照组显著增加(***p<0.001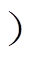 ;当乙醇浓度为20%时,PAES灭活MRSA可使其CFU降低5个数量级以上,即培养基上的细菌菌落数从5×107CFU·mL-1降低到检测域限(1× 102CFU·mL-1)。进一步地,发现当乙醇浓度为5%~20%时,放电情况下PAES的灭菌效果相较于不放电情况下乙醇溶液的灭菌效果显著增加(&&p<0.01,&&&p<0.001)。以上分析结果表明,Ar等离子体射流和乙醇溶液确实具有协同灭菌效应。
;当乙醇浓度为20%时,PAES灭活MRSA可使其CFU降低5个数量级以上,即培养基上的细菌菌落数从5×107CFU·mL-1降低到检测域限(1× 102CFU·mL-1)。进一步地,发现当乙醇浓度为5%~20%时,放电情况下PAES的灭菌效果相较于不放电情况下乙醇溶液的灭菌效果显著增加(&&p<0.01,&&&p<0.001)。以上分析结果表明,Ar等离子体射流和乙醇溶液确实具有协同灭菌效应。
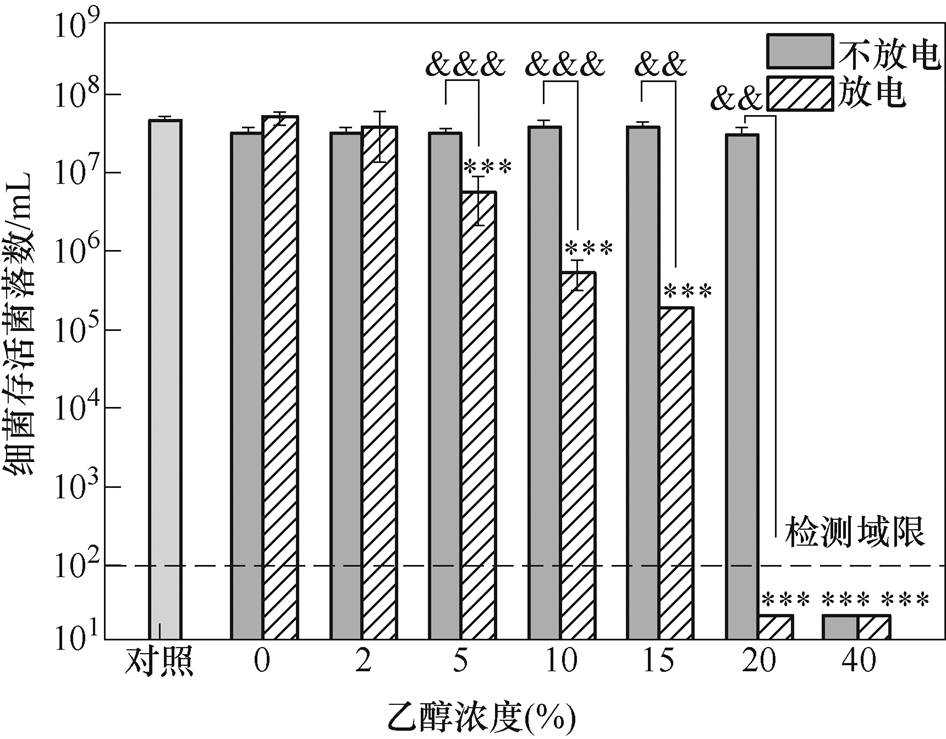
图2 放电和不放电两种情况下PAES和乙醇溶液对MRSA的灭活效果
Fig.2 Inactivation effect of PAES and ethanol solution on MRSA with and without discharge
由于20%乙醇对于伤口的刺激性仍较大,为了降低乙醇对伤口的刺激性,同时增强PAES的灭菌效果,本小节进一步研究了工作气体中不同O2或N2掺杂浓度对灭菌效果的影响。
工作气体Ar中不同O2或N2掺杂浓度下PAES对MRSA的灭活效果如图3所示。当工作气体Ar中掺杂O2后,PAES反而失去对MRSA的灭活效果,如图3a所示。原因可能是电负性氧气大量吸附等离子体中的电子,从而影响等离子体射流与乙醇溶液的相互作用。当工作气体Ar中掺杂N2时,PAES的灭菌效果随着乙醇浓度的增加逐渐增强,随着N2浓度的增加先增强后减弱,如图3b所示。其中,当N2掺杂浓度为0.2%时,PAES的灭菌效果最佳,此时在2%乙醇浓度条件下就能实现5个数量级以上灭菌效果的增强。原因可能是少量的N2掺杂可以促进RNS的产生,而较高浓度的N2掺杂使得电子与N2的碰撞电离加剧,对放电特性产生较大影响,从而影响等离子体射流与水溶液的相互作用。
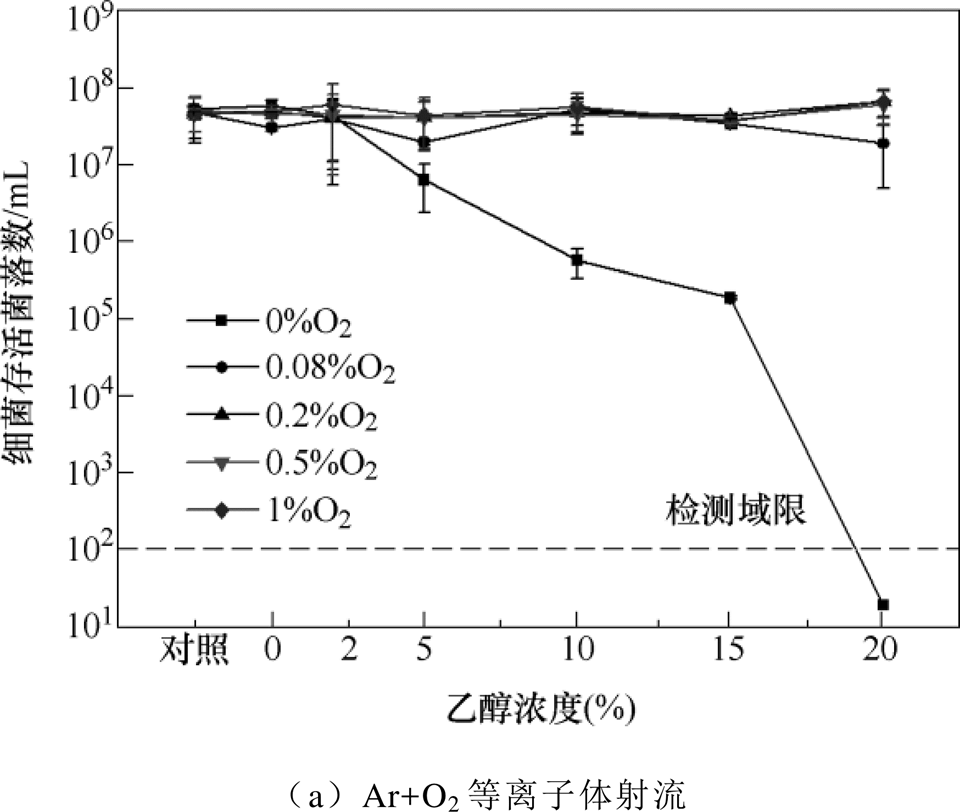
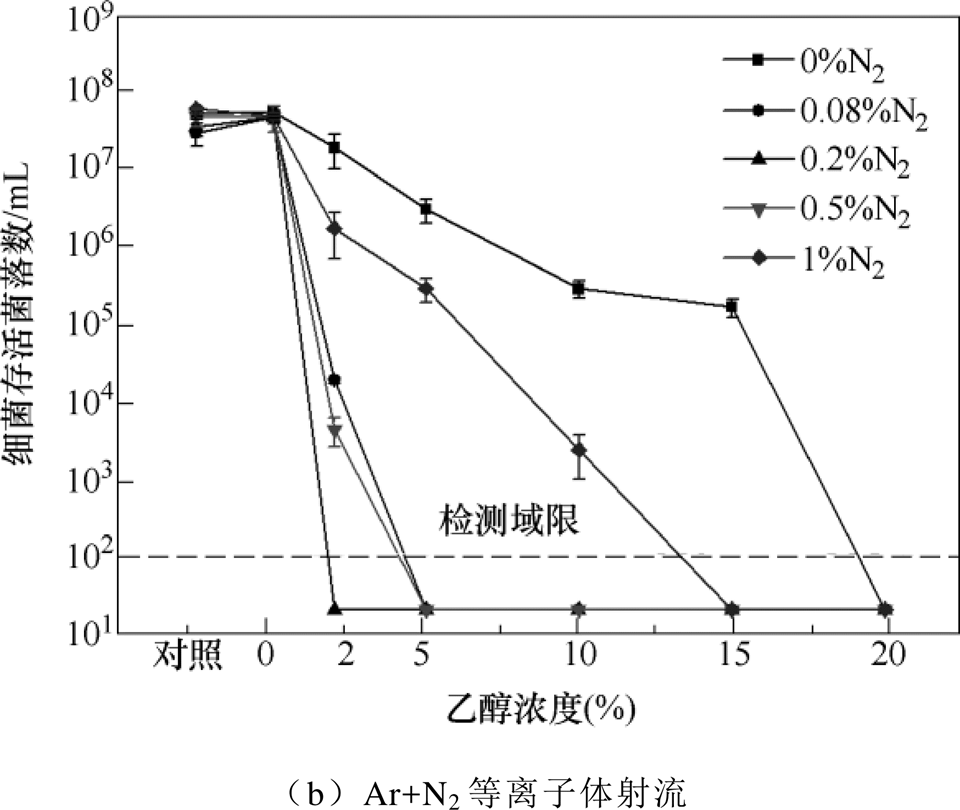
图3 工作气体Ar中不同O2或N2掺杂浓度下PAES对MRSA的灭活效果
Fig.3 Inactivation effect of PAES on MRSA under different O2 or N2 doping concentrations in Ar
图4展示了Ar等离子体射流处理2%乙醇溶液的电压电流波形。在电压波形上升沿和下降沿处,电流波形的放大图像为多条抖动的曲线(此处用三条曲线进行示意)。这表明即使在纳秒脉冲电压的激励下,Ar等离子体射流的电流波形仍不稳定,即Ar等离子体射流仍处于丝状放电模式。随着工作气体Ar中O2掺杂浓度的增加(0~1%),电流波形变得更加不稳定,这说明O2的掺杂不利于Ar等离子体射流的弥散化。随着工作气体Ar中N2掺杂浓度的增加(0~1%),电流波形仍不稳定(由于掺杂O2或N2后Ar等离子体射流的电流波形都不稳定,且和图4相似,没有给出它们的电压电流波形)。
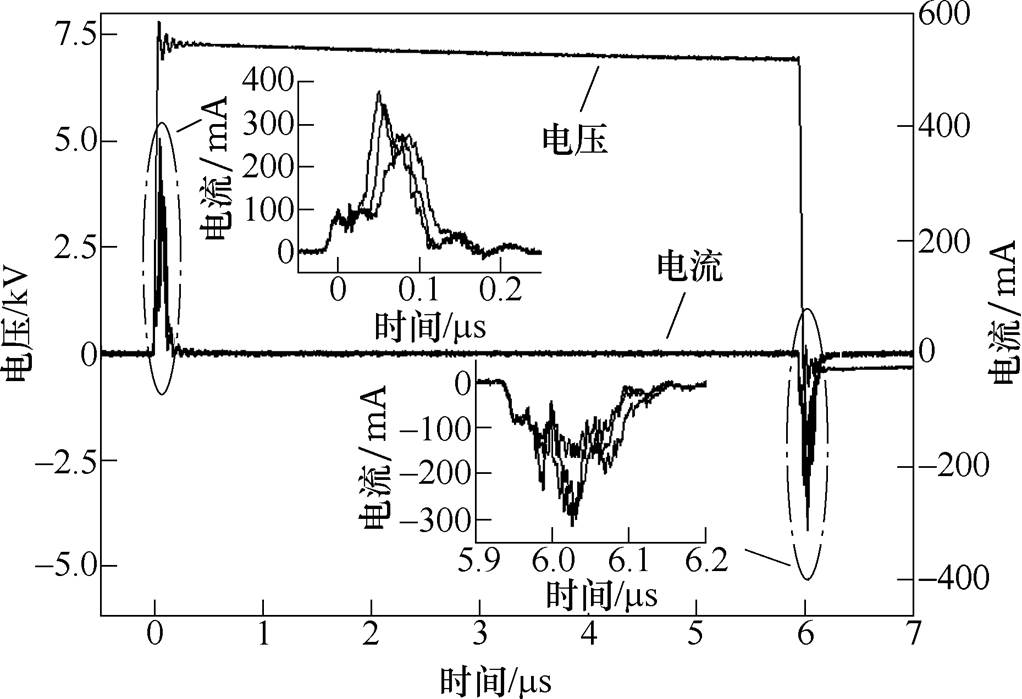
图4 Ar等离子体射流处理2%乙醇溶液的电压电流波形
Fig.4 Voltage and current waveforms of 2% ethanol solution treated by Ar plasma jet
图5展示了工作气体Ar中不同O2或N2掺杂浓度下等离子体射流处理2%乙醇溶液的放电图像。随着工作气体Ar中O2掺杂浓度的逐渐增加(0~1%),Ar+O2等离子体羽流的长度逐渐变短。甚至当O2掺杂浓度为1%时,等离子体羽流不能喷出石英管的管口。而随着工作气体Ar中N2掺杂浓度的逐渐增加(0~1%),Ar+N2等离子体羽流的形态没有发生明显改变,且都能作用于乙醇溶液。原因是电负性的O2具有较高的电子亲和势(0.45eV),吸附了大量电子,从而阻碍了等离子体羽流向前传播,导致等离子体羽流长度变短。而掺杂O2和N2后等离子羽流长度的差异可能导致PAES灭菌效果的不同。
为了研究Ar+O2/N2等离子体射流与乙醇溶液相互作用的动态过程,通过ICCD相机拍摄了Ar+ O2/N2等离子体射流处理2%乙醇溶液的短时间曝光图像。
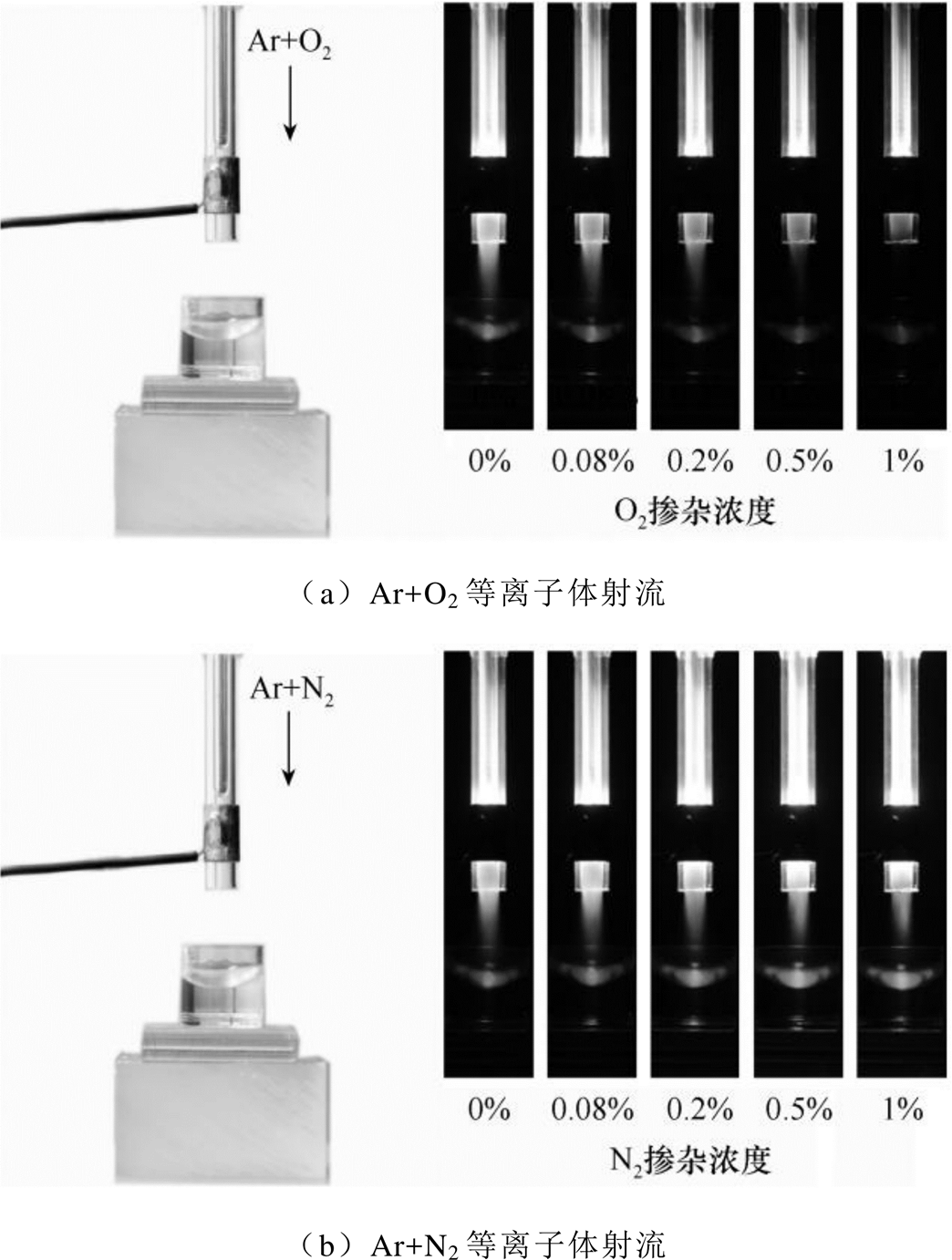
图5 工作气体Ar中掺杂不同O2或N2浓度时等离子体射流处理2%乙醇溶液的放电图像
Fig.5 Discharge images of 2% ethanol solution treated by plasma jet under different O2 or N2 doping concentrations
图6a展示了Ar+O2等离子体射流处理2%乙醇溶液的等离子体时空演化过程。随着O2掺杂浓度的升高,等离子体持续时间逐渐变短;当O2浓度为0.2%时,等离子体不能作用到液面;当O2浓度为1%时,等离子体不能喷出石英管管口。结合图3a灭菌效果,分析认为,等离子体射流作用到液面的持续时间可能是影响灭菌效果的重要因素。图6b展示了Ar+N2等离子体射流处理2%乙醇溶液的等离子体时空演化过程。随着N2掺杂浓度的增加(0~1%),等离子体在空气中传播的持续时间稍微变短(1 250ns→1 050ns),且仍一直能作用到液面。
由于液相活性粒子可以通过气相活性粒子传质到水溶液中,并与水分子、有机溶质(主要是乙醇)、无机溶质(溶解O2、N2等)等反应产生,本节对气液界面激发态粒子的发射光谱进行了检测与分析。

图6 Ar+O2/N2等离子体射流处理2%乙醇溶液的等离子体时空演化图像
Fig.6 Spatial-temporally resolved images of 2% ethanol solution treated by Ar+O2/N2 plasma jet
图7展示了Ar等离子体射流处理2%乙醇溶液时气液交界面处的发射光谱,主要包括OH谱带(306~312nm)及其衍射带、氮分子第二正带系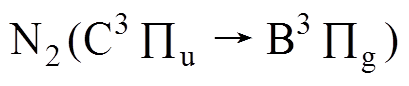 及其衍射带、Ar原子谱线。OH谱带在309nm处具有最大的发射强度。氮分子第二正带系对应于电子态(
及其衍射带、Ar原子谱线。OH谱带在309nm处具有最大的发射强度。氮分子第二正带系对应于电子态(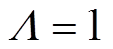 )
)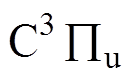 (11.1eV)与
(11.1eV)与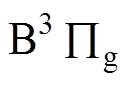 (7.39eV)之间的辐射跃迁。其中波长为337nm的谱线为氮分子激发态
(7.39eV)之间的辐射跃迁。其中波长为337nm的谱线为氮分子激发态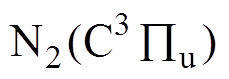 自发跃迁到较低的能态
自发跃迁到较低的能态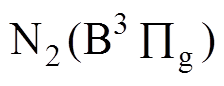 产生的谱线,且在氮分子第二正带系中具有最大的发射强度,即
产生的谱线,且在氮分子第二正带系中具有最大的发射强度,即
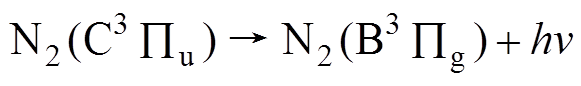 (1)
(1)式中,hv为光子。Ar原子谱线则集中在690~800nm这一范围内,都是属于4p→3s的跃迁。其中,波长为696.5nm的Ar原子谱线,即Ar原子从2P2激发态跃迁到1S5亚稳态的谱线,具有最大的发射强度。
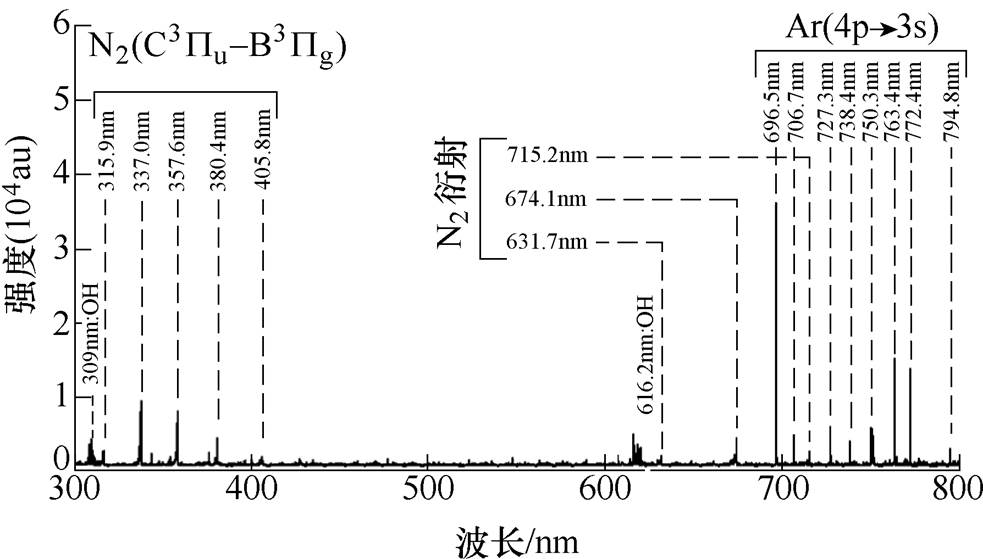
图7 Ar等离子体射流处理2%乙醇溶液时气液界面处的发射光谱
Fig.7 Emission spectrum at the gas-liquid interface of 2% ethanol solution treated by Ar plasma jet
进一步地,研究了气液界面处激发态粒子OH(309nm)、N2(337nm)、Ar(696.5nm)的发射强度随工作气体Ar中O2和N2掺杂浓度的变化。随着O2掺杂浓度的升高,OH(309nm)、N2(337nm)、Ar(696.5nm)的发射强度都逐渐降低,如图8a所示。随着N2掺杂浓度的升高,Ar(696.5nm)和OH(309nm)的发射强度都逐渐降低,而N2(337nm)的发射强度逐渐升高,如图8b所示。
当工作气体Ar中掺杂O2后,PAES反而失去了对MRSA的灭活效果。通过放电特性和发射光谱分析发现,工作气体Ar中O2的掺杂使得等离子体作用不到液面,同时气液界面各种激发态粒子的发射强度也降低。由于工作气体中掺杂电负性O2对放电特性和激发态粒子的负面影响较大,同时O2对液相ROS和RNS的生成又不可或缺,本节通过在石英屏蔽罩中通入Ar+O2,研究了环境气体中不同O2浓度对Ar等离子射流活化乙醇溶液灭菌效果的影响,实验装置如图9所示。石英屏蔽罩置于聚四氟乙烯胶垫上,体积为5cm×5cm×5cm。通入石英屏蔽罩的Ar+O2流速为5L/min。
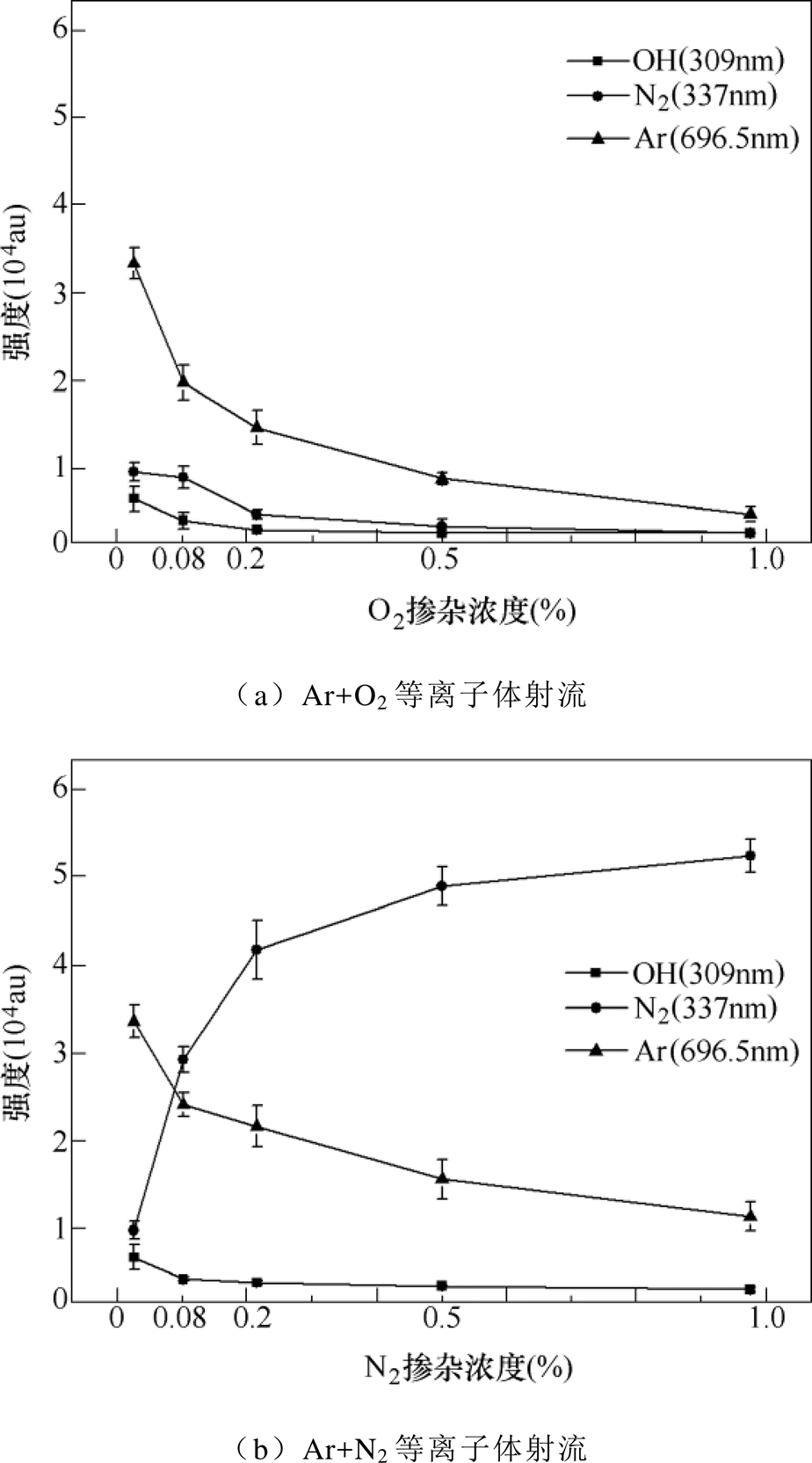
图8 气液界面处激发态粒子的发射强度随工作气体Ar中不同O2或N2掺杂浓度的变化
Fig.8 Emission intensity of radiative species at gas-liquid interface with different O2 or N2 doping concentrations
屏蔽罩中通入Ar+O2时Ar等离子体射流处理2%乙醇溶液的放电图像如图10所示。当石英屏蔽罩中通入Ar+O2后,随着环境气体中O2掺杂浓度的升高(0~1%),Ar等离子体射流的羽流形态变化不大,且等离子体羽流都能作用到液面。相比于在工作气体中掺杂O2(见图5a),环境气体中相同浓度的O2掺杂对等离子体羽流的影响较小。
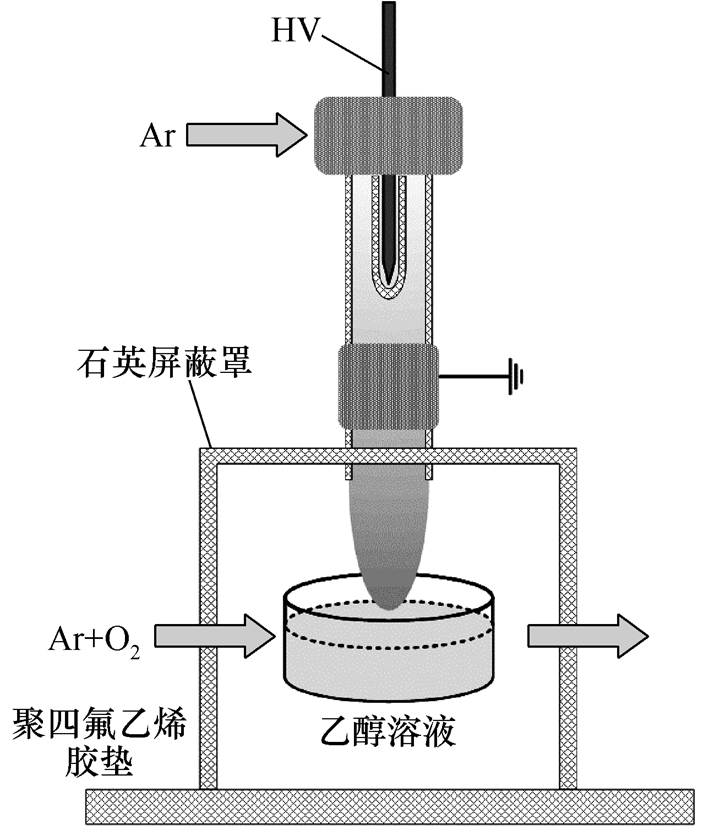
图9 Ar等离子体射流处理乙醇溶液且石英屏蔽罩中通入Ar+O2的实验装置
Fig.9 Experimental setup of ethanol solution treated by Ar plasma jet with Ar+O2 in shield

图10 屏蔽罩中通入Ar+O2时Ar等离子体射流处理2%乙醇溶液的放电图像
Fig.10 Discharge images of 2% ethanol solution treated by Ar plasma jet with Ar+O2 in shield
图11展示了在屏蔽罩中通入Ar+O2后,不同O2掺杂浓度下Ar等离子体射流处理2%乙醇溶液的时空演化过程。结果表明,随着O2掺杂浓度的升高(0~1%),Ar等离子体都能作用到液面,且Ar等离子体射流作用到液面的持续时间远大于未添加屏蔽罩的情况(见图6a)。特别是当O2掺杂浓度为1%时,在屏蔽罩中通入Ar+O2情况下,Ar等离子体射流作用到液面的持续时间约为400ns,而不加屏蔽罩情况下,Ar+O2等离子体射流不能从管口喷出。
值得注意的是,在添加屏蔽罩的情况下,等离子体中出现多个放电通道交叠的现象,如T=850ns时Ar等离子体的图像。由于亚稳态Ar*(43P20)的势能为11.56eV,而气液界面的乙醇气体分子的电离能只有10.47eV,Ar*和乙醇气体分子在气液界面发生彭宁电离的概率很大[27-29],有
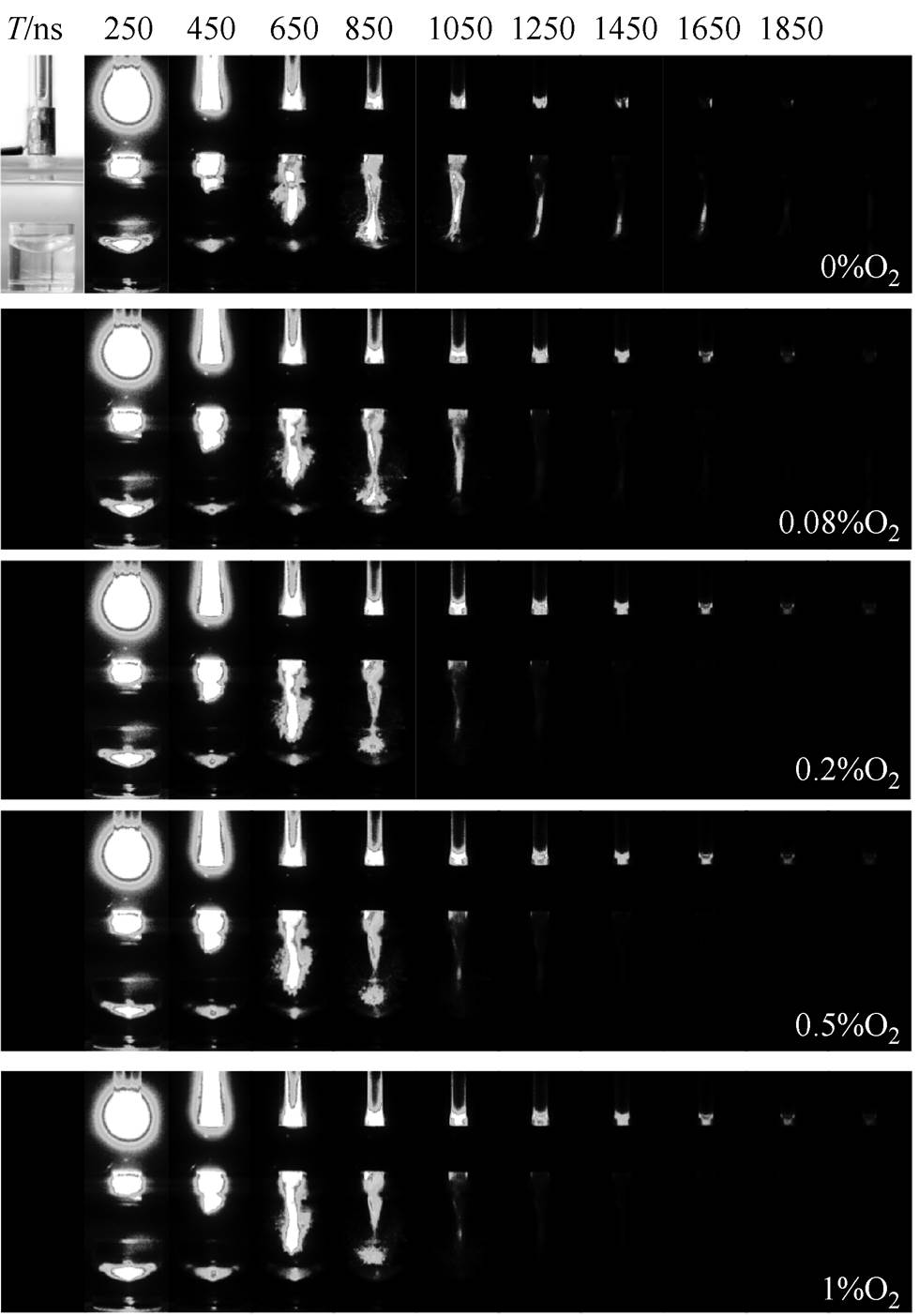
图11 屏蔽罩中通入Ar+O2时Ar等离子体射流处理2%乙醇溶液的等离子体时空演化图像
Fig.11 Spatial-temporally resolved images of 2% ethanol solution treated by Ar plasma jet with Ar+O2 in shield
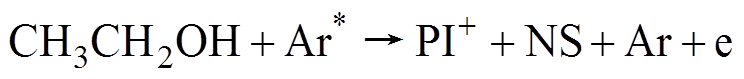 (2)
(2)式中,PI+为正离子;NS为中性粒子;e为电子。因此,Ar*和乙醇气体分子在气液界面的彭宁电离可能导致了等离子体中多个放电通道的交叠。
图12展示了气液界面处激发态粒子OH(309nm)、N2(337nm)、Ar(696.5nm)的发射强度随屏蔽罩中O2掺杂浓度的变化。随着O2掺杂浓度的升高,Ar(696.5nm)发射强度略微下降,OH(309nm)的发射强度逐渐下降,此时基本检测不到N2(337nm)的发射强度。
图13展示了当屏蔽罩中不同O2掺杂浓度时Ar射流等离子体活化乙醇溶液对MRSA的灭活效果。随着屏蔽罩中O2掺杂浓度的增加(0~1%),PAES的灭菌效果逐渐增加,且当屏蔽罩中O2掺杂浓度为1%时,被处理的水溶液中掺杂2%乙醇浓度就能实现5个数量级以上的灭菌效果增强。值得注意的是,随着通入屏蔽罩中的O2浓度从0增加到1%,Ar(696.5nm)的发射强度从4.5×104(au)降为3.9×104 (au)(电负性O2掺杂浓度增加导致其含量稍微降低),而灭菌效果却从无灭活效果增加到5个数量级以上的灭活效果。由于只有O2浓度发生较大改变,这说明O2是影响灭菌效果的关键因素。
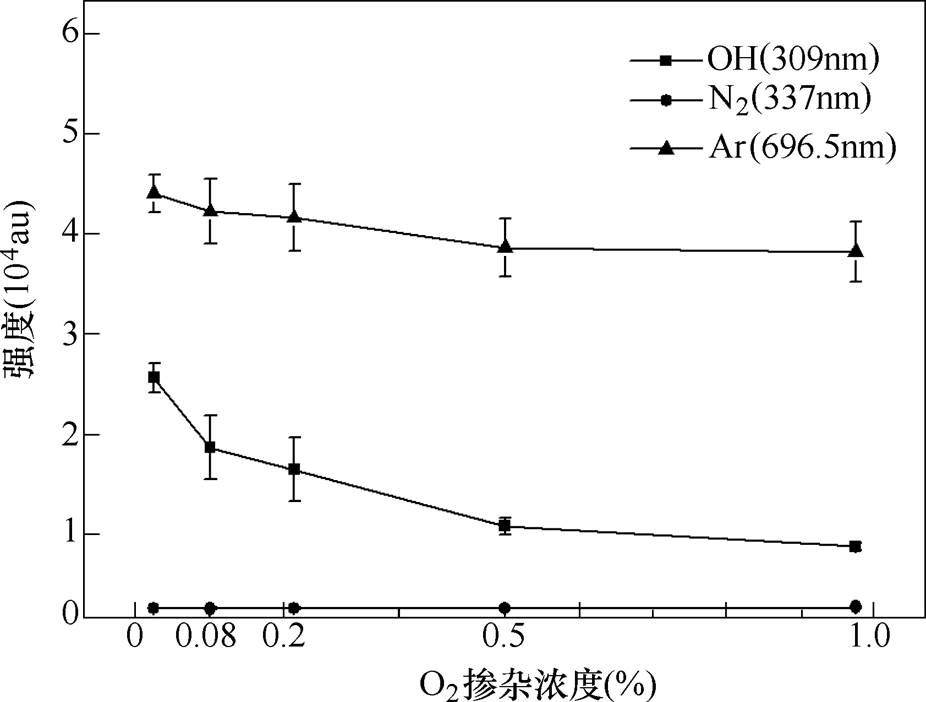
图12 气液界面处激发态粒子的发射强度随屏蔽罩中O2掺杂浓度的变化
Fig.12 Emission intensity of radiative species at gas-liquid interface with O2 doping in shield
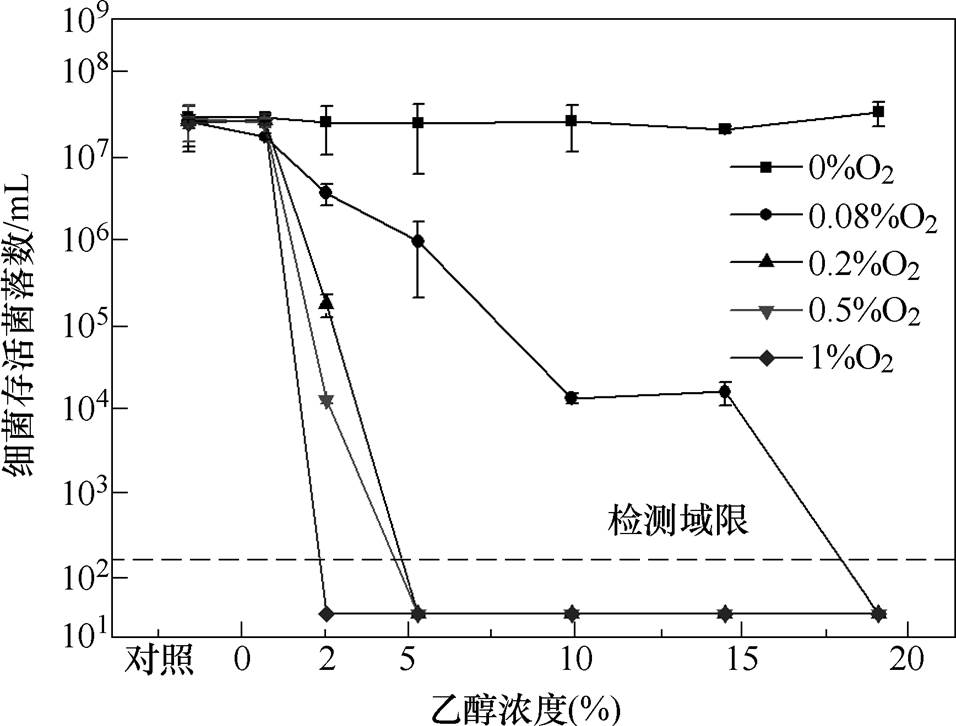
图13 屏蔽罩中不同O2掺杂浓度下PAES对MRSA的灭活效果
Fig.13 Inactivation effect of PAES on MRSA with different O2 doping concentrations in shielding
由于灭菌实验中采用的是PAES间接灭活MRSA,等离子体活化乙醇溶液中可能存在一种或几种起关键灭菌作用的长寿命活性粒子。图14展示了PAES中活性粒子的色谱和负离子质谱。结果表明,PAES中主要包括m/z分别为62、73、75和89的负离子。对于m/z=62的负离子,其可能是NO3-和·ONOO-。·ONOO-本身是一种短寿命的活性粒子,在液相中的半衰期仅1s左右,但是在酸性条件下可以通过H2O2与NO2-/HNO2反应生成。虽然这个反应的反应速率系数较低(0.56M-1s-1),但是由于其来源于溶液中两种能够稳定存在的长寿命粒子,因此这个反应存在较高的发生可能性。Chen Chen等[30]和P. Lukes等[31]的实验结果也验证了这一过程的存在。对于m/z=75的负离子,其可能包含CH3COOO-。Xia Wenjie等的研究结果[20]表明,等离子体活化水中寿命为3~10min的过氧乙酸(CH3COOOH)可能是关键的灭菌物质。
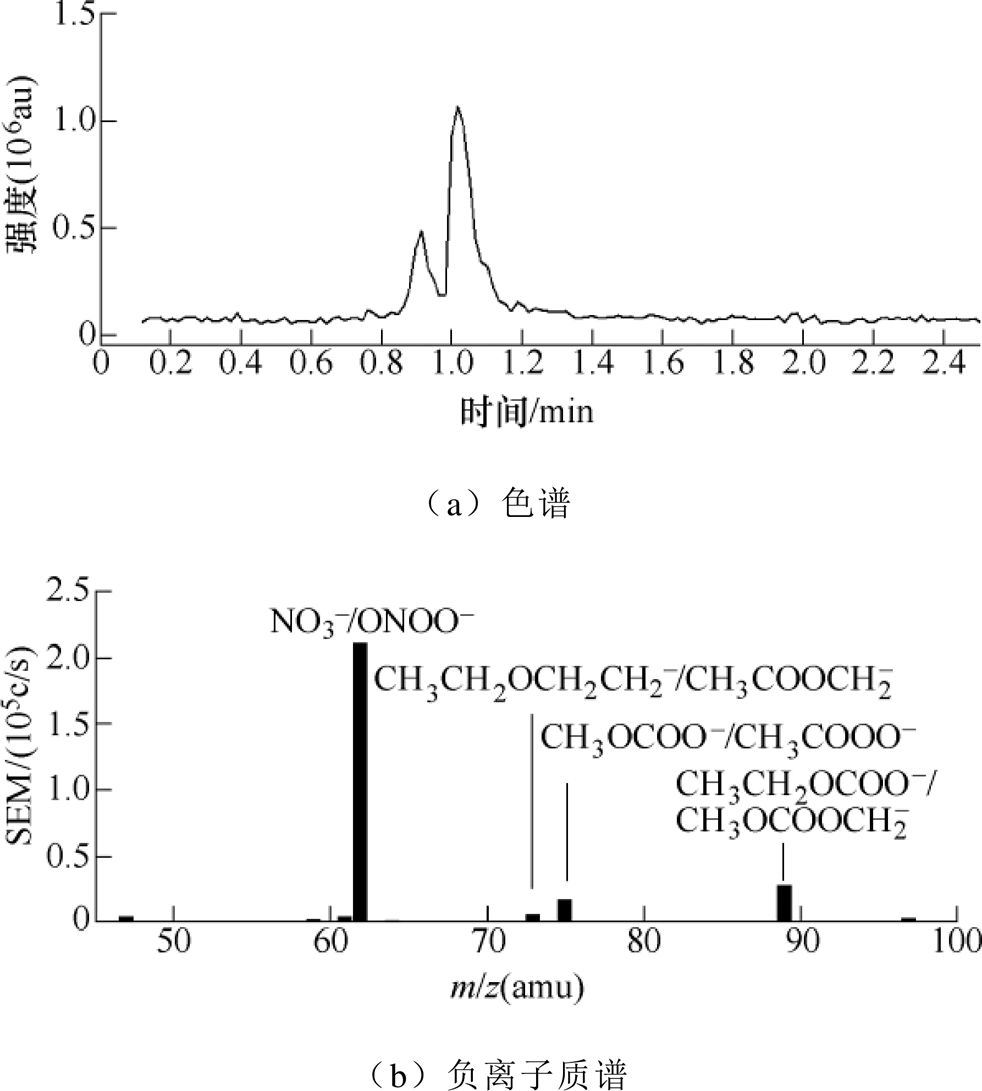
图14 PAES中活性粒子的色谱和负离子质谱
Fig.14 Chromatography and negative ion mass spectra of reactive species in PAES
将PAES静置30min后,发现PAES对MRSA基本没有灭活效果,推测PAES中起关键灭菌作用的液相粒子可能是一种或几种较长寿命的不稳定粒子。图15比较了PAES未静置和静置30min后m/z分别为62、73、75和89的负离子色谱。
结果表明,在静置30min后,m/z=62的色谱峰强度增加。原因可能是亚硝酸通过反应式(3)和式(4)转变为硝酸[32],有
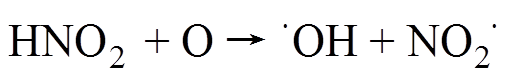 (3)
(3)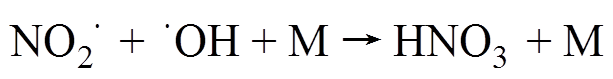 (4)
(4)
还可能是过氧化亚硝酸通过反应式(5)分解为高化学活性的·OH和NO2·自由基,再通过反应式(4)转变为硝酸[31],有
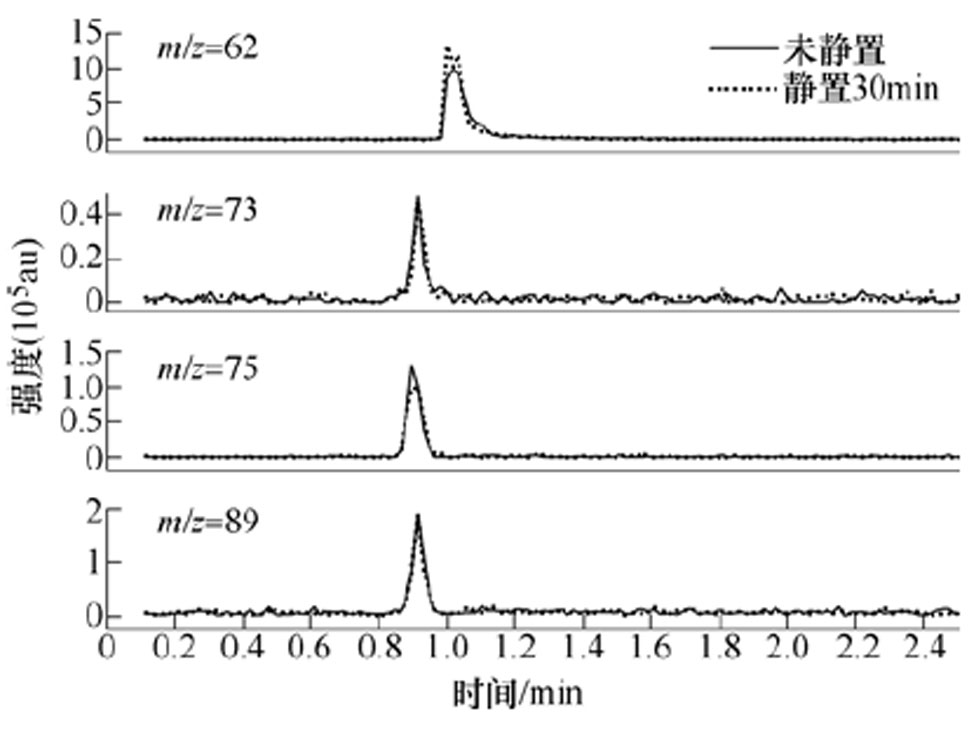
图15 未静置和静置30min后PAES中不同m/z负离子的色谱
Fig.15 Chromatogram of negative ions with different m/z in PAES without standing and after standing for 30min
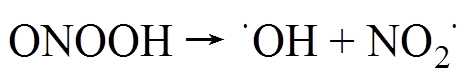 (5)
(5)P. Lukes等认为反应式(5)产生的·OH和NO2·自由基在细菌灭活中起着关键的作用[33]。同时,实验结果发现,在静置30min后,m/z=75的色谱峰强度降低。这进一步表明PAES中可能存在过氧乙酸。研究表明,过氧乙酸主要通过过氧化物基团攻击细胞膜、氧化氨基酸、损伤核酸等方式对微生物进行灭活[34]。
图16展示了三种处理情况下等离子体活化2%乙醇溶液中TEMPONE·浓度、m/z=75的色谱峰面积以及细菌存活菌落数随O2/N2掺杂浓度的变化。由于捕捉剂TEMPONE-H是在等离子体射流处理乙醇溶液之后加入,TEMPONE-H主要与PAES中的·ONOO-反应生成自旋加合物TEMPONE·,即TEMPONE·浓度主要指的是过氧亚硝酸的浓度。 m/z=75的色谱峰面积用来表征质荷比为75的负离子浓度,一定程度上反映了过氧乙酸的浓度。不同于Ar+O2等离子体射流处理乙醇溶液,在屏蔽罩中通入Ar+O2后PAES中的TEMPONE·浓度随着O2掺杂浓度升高先缓慢增加,之后维持在5mM左右;而m/z=75的色谱峰面积随着O2掺杂浓度升高逐渐增大,此时灭菌效果也逐渐增加(见图16a和图16c)。这表明Ar等离子体射流处理乙醇溶液且屏蔽罩中通Ar+O2时,过氧乙酸可能在灭菌过程中起主导作用。对于Ar+N2等离子体射流处理乙醇溶液,TEMPONE·浓度随着N2掺杂浓度升高先增后减,且在0.08%N2掺杂浓度条件下有最大值约为22mM;m/z=75的色谱峰面积也随着N2掺杂浓度升高先增后减,但在0.2%N2掺杂浓度条件下有最大值;而灭菌效果也随着N2掺杂浓度升高先增后减,且在0.2%N2掺杂浓度条件下最强(见图16b)。这进一步说明过氧乙酸可能在灭菌中起着关键作用,而过氧亚硝酸和过氧乙酸可能具有协同灭菌作用。
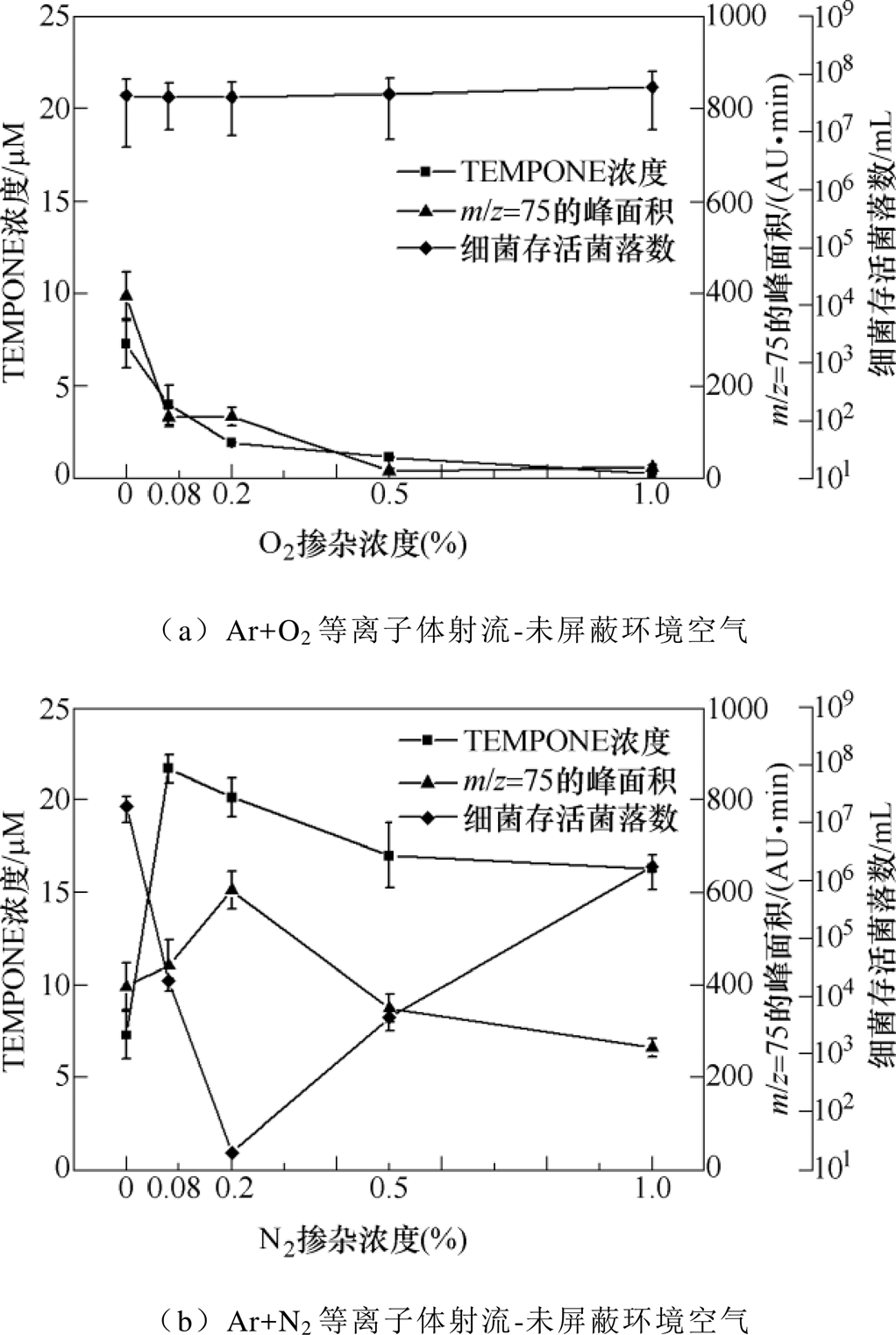
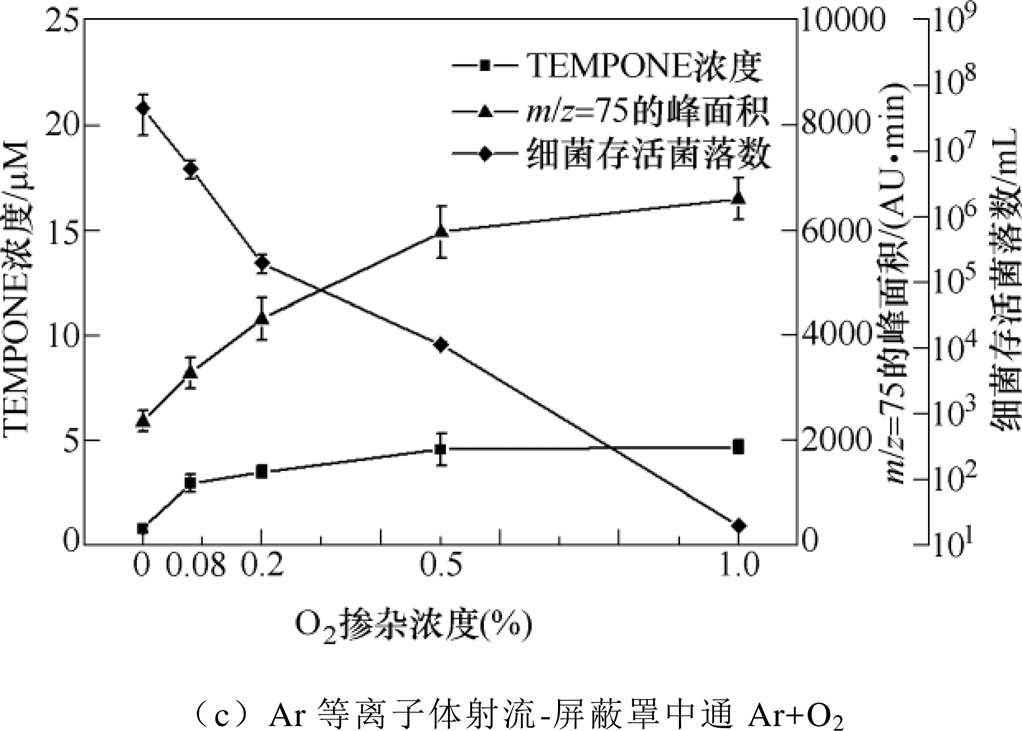
图16 三种处理情况下等离子体活化2%乙醇溶液中TEMPONE·浓度、m/z=75的色谱峰面积以及细菌存活菌落数随O2/N2掺杂浓度的变化
Fig.16 Concentration of TEMPONE·, chromatographic peak area with m/z=75, and surviving CFU in 2%PAES with O2/N2 doping concentration under three conditions
本文研究了Ar等离子体射流处理水溶液中少量乙醇掺杂对放电特性和灭菌效应的影响规律。首先,发现Ar等离子体射流和乙醇溶液具有协同灭菌效应,且在被处理的水溶液中掺杂20%乙醇溶液可使等离子体活化水的灭菌效果提高5个数量级以上。其次,发现在工作气体中掺杂O2不利于灭菌效果的提升;而当工作气体Ar中掺杂0.2%N2时,只需在被处理的水溶液中掺杂2%乙醇,即可使等离子体活化水的灭菌效果提高5个数量级以上。通过放电特性和发射光谱的分析,发现等离子体作用于液面的持续时间和气液界面激发态粒子的发射强度是影响灭菌效果的重要因素。进而提出了在屏蔽罩中通入Ar+O2以优化Ar射流等离子体活化乙醇溶液灭菌效果的方法,发现当屏蔽罩中掺杂1%O2时,在被处理的水溶液中掺杂2%乙醇即可提高5个数量级以上的灭菌效果。同时,发现2%乙醇掺杂可使等离子体中多个放电通道交叠,原因可能是亚稳态Ar*和乙醇气体分子在气液界面的彭宁电离作用。最后,阐述了等离子体活化乙醇溶液中过氧乙酸可能在灭菌过程中起主导作用,而过氧亚硝酸和过氧乙酸可能协同作用增强灭菌效果。
参考文献
[1] Kong M G, Kroesen G, Morfill G, et al. Plasma medicine: an introductory review[J]. New Journal of Physics, 2009, 11(11): 115012.
[2] Weltmann K D, Woedtke T V. Plasma medicine- current state of research and medical application[J]. Plasma Physics and Controlled Fusion, 2017, 59(1): 014031.
[3] Lu Xinpei, Reuter S, Laroussi M, et al. Nonequili- brium atmospheric pressure plasma jets: funda- mentals, diagnostics, and medical applications[M]. Boca Raton: CRC Press, 2019.
[4] Morfill G E, Kong M G, Zimmermann J L. Focus on plasma medicine[J]. New Journal of Physics, 2009, 11(11): 115011.
[5] Von W T, Reuter S, Masur K, et al. Plasmas for medicine[J]. Physics Report, 2013, 530(4): 291-320.
[6] 徐晗, 陈泽煜, 刘定新. 大气压冷等离子体处理水溶液: 液相活性粒子检测方法综述[J]. 电工技术学报, 2020, 35(17): 3561-3582.
Xu Han, Chen Zeyu, Liu Dingxin. Aqueous solutions treated by cold atmospheric plasmas: a review of the detection methods of aqueous reactive species[J]. Transactions of China Electrotechnical Society, 2020, 35(17): 3561-3582.
[7] 孔刚玉, 刘定新. 气体等离子体与水溶液的相互作用研究—意义、挑战与新进展[J]. 高电压技术, 2014, 40(10): 2956-2965.
Kong Gangyu, Liu Dingxin. Researches on the inter- action between gas plasmas and aqueous solutions: significance, challenges and new progresses[J]. High Voltage Engineering, 2014, 40(10): 2956-2965.
[8] Sato T, Furuya O, Ikeda K, et al. Generation and transportation mechanisms of chemically active species by dielectric barrier discharge in a tube for catheter sterilization[J]. Plasma Processes and Polymers, 2008, 5(6): 606-614.
[9] Guo Li, Zhao Yiming, Liu Dingxin, et al. Cold atmospheric-pressure plasma induces DNA-protein crosslinks through protein oxidation[J]. Free Radical Research, 2018, 52(7): 783-798.
[10] Xu Han, Liu Dingxin, Xia Wenjie, et al. Comparison between the water activation effects by pulsed and sinusoidal helium plasma jets[J]. Physics of Plasmas, 2018, 25(1): 013520.
[11] 张若兵, 徐莹, 张驰, 等. 双脉冲放电等离子体水处理H2O2的生成规律[J]. 高电压技术, 2010, 36(9): 2297-2302.
Zhang Ruobing, Xu Ying, Zhang Chi, et al. Formation of hydrogen peroxide by bipolar pulsed discharge plasma in water[J]. High Voltage Engineering, 2010, 36(9): 2297-2302.
[12] Chen Zeyu, Cui Qingjie, Chen C hen, et al. Inactivation of myeloma cancer cells by helium and argon plasma jets: the effect comparison and the key reactive species[J]. Physics of Plasmas, 2018, 25(2): 023508.
[13] Reuter S, Winter J, Iséni S, et al. The influence of feed gas humidity versus ambient humidity on atmospheric pressure plasma jet-effluent chemistry and skin cell viability[J]. IEEE Transactions on Plasma Science, 2014, 43(9): 3185-3192.
[14] He Tongtong, Liu Dingxin, Liu Zhijie, et al. The mechanism of plasma-assisted penetration of NO2-in model tissues[J]. Applied Physics Letters, 2017, 111(20): 203702.
[15] Liu Dingxin, Liu Zhichao, Chen Chen, et al. Aqueous reactive species induced by a surface air discharge: heterogeneous mass transfer and liquid chemistry pathways[J]. Scientific Reports, 2016, 6(1): 23737.
[16] Ikawa S, Tani A, Nakashima Y, et al. Physico- chemical properties of bactericidal plasma-treated water[J]. Journal of Physics D: Applied Physics, 2016, 49(42): 425401.
[17] 吴淑群, 董熙, 裴学凯, 等. 基于激光诱导荧光法诊断大气压低温等离子体射流中OH自由基和O原子的时空分布[J]. 电工技术学报, 2017, 32(8): 82-94.
Wu Shuqun, Dong Xi, Pei Xuekai, et al. Laser induced fluorescence diagnostics of the temporal and spatial distribution of OH radicals and O atom in a low temperature plasma jet at atmospheric pressure[J]. Transactions of China Electrotechnical Society, 2017, 32(8): 82-94.
[18] Ma Ruonan, Wang Guoming, Tian Ying, et al. Non-thermal plasma- activated water inactivation of food-borne pathogen on fresh produce[J]. Journal of Hazardous Materials, 2015, 300: 643-651.
[19] Xu Yingyin, Tian Ying, Ma Ruonan, et al. Effect of plasma activated water on the postharvest quality of button mushrooms, agaricus bisporus[J]. Food Chemistry, 2016, 197: 436-444.
[20] Xia Wenjie, Liu Dingxin, Guo Li, et al. Discharge characteristics and bactericidal mechanism of Ar plasma jet with ethanol and oxygen gas admixtures[J]. Plasma Sources Science and Technology, 2019, 28(12): 125005.
[21] 张波, 汪立峰, 刘峰, 等. 交流和纳秒脉冲激励氦气中等离子体射流阵列放电特性比较[J]. 电工技术学报, 2019, 34(6): 1319-1328.
Zhang Bo, Wang Lifeng, Liu Feng, et al. Comparison on discharge characteristics of the helium plasma jet array excited by alternating current and nanosecond pulse voltage[J]. Transactions of China Electro- technical Society, 2019, 34(6): 1319-1328.
[22] 赵勇, 王瑞雪, 章程, 等. 脉冲波形对氦等离子体射流子弹传播特性的影响[J]. 电工技术学报, 2019, 34(16): 3472-3479.
Zhao Yong, Wang Ruixue, Zhang Cheng, et al. The effect of pulse parameters on helium plasma bullet distribution properties[J]. Transactions of China Electrotechnical Society, 2019, 34(16): 3472-3479.
[23] 周亦骁, 方志, 邵涛. Ar/O2和Ar/H2O中大气压等离子体射流放电特性的比较[J]. 电工技术学报, 2014, 29(11): 229-238.
Zhou Yixiao, Fang Zhi, Shao Tao. Comparison of discharge characteristics of atmospheric pressure plasma jet in Ar/O2 and Ar/H2O mixtures[J]. Transa- ctions of China Electrotechnical Society, 2014, 29(11): 229-238.
[24] 张迅, 曾华荣, 田承越, 等. 大气压等离子体制备超疏水表面及其防冰抑霜研究[J]. 电工技术学报, 2019, 34(24): 5289-5296.
Zhang Xun, Zeng Huarong, Tian Chengyue, et al. Super-hydrophobic surface prepared by atmospheric- pressure plasma and its anti-icing, anti-frosting performance[J]. Transactions of China Electro- technical Society, 2019, 34(24): 5289-5296.
[25] 丁正方, 方志, 许靖. 四氟化碳含量对大气压Ar等离子体射流放电特性的影响[J]. 电工技术学报, 2016, 31(7): 159-165.
Ding Zhengfang, Fang Zhi, Xu Jing. Influences of CF4 content on discharge characteristics of argon plasma jet under atmospheric pressure[J]. Transa- ctions of China Electrotechnical Society, 2016, 31(7): 159-165.
[26] 米彦, 苟家喜, 刘露露, 等. 脉冲介质阻挡放电等离子体改性对BN/EP复合材料击穿强度和热导率的影响[J]. 电工技术学报, 2020, 35(18): 3949-3959.
Mi Yan, Gou Jiaxi, Liu Lulu, et al. Effect of pulse dielectric barrier discharge plasma modification on breakdown strength and thermal conductivity of BN/EP composites[J]. Transactions of China Electro- technical Society, 2020, 35(18): 3949-3959.
[27] Glosík J, Pavlík J, Šícha M, et al. A contribution to the study of the influence of metastables in the flowing afterglow plasma[J]. Czechoslovak Journal of Physics, 1987, 37(2): 188-193.
[28] Sun Wenting, Li Guo, Li Heping, et al. Charac- teristics of atmospheric-pressure, radio-frequency glow discharges operated with argon added ethanol[J]. Journal of Applied Physics, 2007, 101(12): 123302.
[29] Xia Wenjie, Liu Dingxin, Xu Han, et al. The effect of ethanol gas impurity on the discharge mode and discharge products of argon plasma jet at atmospheric pressure[J]. Plasma Sources Science and Technology, 2018, 27(5): 055001.
[30] Chen Chen, Li Fanying, Chen Hailan, et al. Aqueous reactive species induced by a PCB surface micro-discharge air plasma device: a quantitative study[J]. Journal of Physics D: Applied Physics, 2017, 50(44): 445208.
[31] Lukes P, Dolezalova E, Sisrova I, et al. Aqueous- phase chemistry and bactericidal effects from an air discharge plasma in contact with water: evidence for the formation of peroxynitrite through a pseudo- second-order post-discharge reaction of H2O2 and HNO2[J]. Plasma Sources Science and Technology, 2014, 23(1): 015019.
[32] Schmidt-Bleker A, Bansemer R, Reuter S, et al. How to produce an NOx- instead of Ox-based chemistry with a cold atmospheric plasma jet plasma[J]. Plasma Processes and Polymers, 2016, 13(11): 1120-1127.
[33] Dolezalova E, Lukes P. Membrane damage and active but nonculturable state in liquid cultures of escherichia coli treated with an atmospheric pressure plasma jet[J]. Bioelectrochemistry, 2015, 103: 7-14.
[34] Wessels S, Ingmer H. Modes of action of three disinfectant active substances: a review[J]. Regulatory Toxicology and Pharmacology, 2013, 67(3): 456- 467.
Discharge Characteristics and Bactericidal Effect of Ar Plasma Jet Treating Ethanol Aqueous Solution
Abstract Ethanol is a kind of commonly used disinfectant in medical treatment. Theoretically, doping ethanol into aqueous solution treated by Ar plasma jet can enhance the bactericidal effect. Through the inactivation experiment of Methicillin-resistant Staphylococcus aureus, it was found that the bactericidal effect of Ar jet plasma-activated water was increased by more than 5 orders of magnitude by doping 20% ethanol. Furthermore, when 0.2% N2 was mixed into the working gas or 1% O2 was added into the shield, the bactericidal effect can be improved by more than 5 orders of magnitude by doping 2% ethanol. At the same time, 2% ethanol doping can cause the overlapping of multiple discharge channels in the plasma, which may be due to Penning ionization of metastable Ar* and ethanol gas molecules at the gas-liquid interface. Finally, the analysis of reactive species in liquid phase show that peracetic acid in ethanol solution activated by plasma may play a leading role in the sterilization process, and peroxynitrite and peracetic acid may synergistically enhance the bactericidal effect.
keywords:Ar plasma jet, ethanol, discharge characteristics, bactericidal effect
中图分类号:TM89
DOI: 10.19595/j.cnki.1000-6753.tces.201227
收稿日期2020-09-17
改稿日期 2020-10-10
夏文杰 男,1991年生,博士,研究方向为大气压冷等离子体射流及其生物医学应用。E-mail: 690726712@qq.com
刘定新 男,1982年生,博士,博士生导师,研究方向为大气压冷等离子体技术及其生物医学应用、放电设备故障诊断等。E-mail: liudingxin@mail.xjtu.edu.cn(通信作者)
(编辑 崔文静)